题目内容
【题目】某实验小组用下图装置制备家用消毒液,并探究其性质。
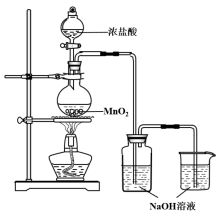
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
a. 测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
b. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(1)写出利用上述装置制备消毒液涉及反应的化学方程式 、 。
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有 性。
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因: (用离子方程式表示)。
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是 。
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32- + I2 === S4O62- + 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是 。
②此消毒液有效氯含量为 %(保留一位有效数字)。获得结论:此实验制得的消毒液 (填“符合”或“不符合”)家用要求。
【答案】(1)4HCl + MnO2 ![]() Cl2↑ + MnCl2 + 2H2O、Cl2 + 2NaOH === NaClO + NaCl + H2O
Cl2↑ + MnCl2 + 2H2O、Cl2 + 2NaOH === NaClO + NaCl + H2O
(2) 5mL pH = 13 ;漂白性
(3)① 2H+ + ClO- + Cl- === Cl2↑+ H2O
② 取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色
(4)① 溶液蓝色褪去② 1.42 % 不符合
【解析】
试题分析:(1)该装置中发生的反应有两个,一个是制取氯气,反应的方程式为4HCl + MnO2 ![]() Cl2↑ + MnCl2 + 2H2O,另一个是氯气与氢氧化钠发生反应制取消毒液,发生反应的方程式为Cl2 + 2NaOH === NaClO + NaCl + H2O。
Cl2↑ + MnCl2 + 2H2O,另一个是氯气与氢氧化钠发生反应制取消毒液,发生反应的方程式为Cl2 + 2NaOH === NaClO + NaCl + H2O。
(2)根据资料可知,酚酞在强碱性溶液中红色会褪去,则为了验证溶液褪色的原因,需要补充碱性溶液使酚酞褪色的对比实验,在这一过程中要注意物质的体积与浓度原溶液相同,所以应取5mL,PH=13的NaOH溶液;通过对比实验的现象,溶液在30min后褪色,与原实验对比5min后褪色证明溶液褪色原因为消毒液的漂白性。
(3)①溶液变成黄绿色的原因为ClO- 与 Cl-在酸性条件下发生氧化还原反应生成了氯气,反应的方程式为2H+ + ClO- + Cl- === Cl2↑+ H2O;②操作b中加入的酸为盐酸,盐酸中含有参与反应的Cl-,所以不严谨,所以补充的实验为将盐酸换成硫酸即可,故答案为取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色。
(4)①用Na2S2O3溶液滴定生成的I2,而这反应的方程式为2S2O32- + I2 === S4O62- + 2I-,则滴定终点的现象为溶液蓝色褪去;②n(Na2S2O3)=20×10-3×0.1=2×10-3mol,2S2O32- + I2 === S4O62- + 2I-,则n(I2)=1/2n(Na2S2O3)=10-3mol,消毒液在酸性条件下与KI反应的离子方程式为4H++2ClO-+2I-=Cl2+I2+2H2O,则n(Cl2)= n(I2)=10-3 mol,则有效氯含量为71×10-3/5=1.42 %<5%,则该消毒液不符合家用要求。

【题目】实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体。
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:___

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)___
仪器标号 | 仪器中所加物质 | 作用 |
A | 亚硫酸钠、浓硫酸 | 产生SO2 |
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液。
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:___。
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量___(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积)。用c、V1、V2表示SO2的体积百分含量为___。