题目内容
19.设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是$\frac{22.4bc}{a{N}_{A}}$L(用含NA的式子表示).分析 根据组分都为氧气,所以其质量与分子数成正比,计算cg气体的物质的量,最后根据气体体积公式求出体积,据此解答.
解答 解:根据其组分都为氧气相同,所以其质量与分子数成正比,ag氧气含有的分子数为:b个,质量与分子数的比列式为:ag:b个=cg:x个,
x=$\frac{bc}{a}$个;
cg该混合气体含有的物质的量为:n=$\frac{bc}{a{N}_{A}}$=mol其体积为:V=n×Vm =$\frac{bc}{a{N}_{A}}$mol×Vm =$\frac{22.4bc}{a{N}_{A}}$L.
故答案为:$\frac{22.4bc}{a{N}_{A}}$L.
点评 本题考查了有关阿伏伽德罗常数的计算,明确相关概念及计算公式是解题关键,题目难度不大.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
10.下列说法不正确的是( )
| A. | 由反应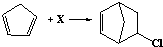 可知,X为氯乙烯 可知,X为氯乙烯 | |
| B. | 异辛烷的结构为(CH3)3CCH2CH(CH3)2,它的一氯代物共有4种同分异构体(不考虑对映异构体),且它们的熔点、沸点各不相同 | |
| C. | 已知CHCl3+HF→CHFCl2+HCl,此反应与由苯制备溴苯的反应类型相同 | |
| D. | 棉、毛、丝、麻完全燃烧时,都只生成CO2和H2O |
7.某同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A. | 所用NaOH已经潮解 | |
| B. | 向容量瓶中加水定容时俯视标线 | |
| C. | 用量筒量取所需的浓盐酸时俯视刻度线 | |
| D. | 定容后倒转容量瓶几次,发现液面最低点低于标线,再补几滴水 |
14.将Na2O2投入H2O中发生的反应为:2Na2O2+2H2O=4NaOH+O2↑.下列说法正确的是( )
| A. | 反应中H2O作还原剂 | |
| B. | Na2O2 和Na2O2 均属于碱性氧化物 | |
| C. | Na2O2晶体中阴、阳离子个数之比为1:1 | |
| D. | 反应中Na2O2既发生氧化反应,又发生还原反应 |
4.亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食能使人中毒.区别食盐和亚硝酸钠的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种有刺激性气味气体的是亚硝酸钠.该气体可能是( )
| A. | NO2 | B. | N2 | C. | NH3 | D. | SO2 |
11.某物质可由两种单质直接化合生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生.下列物质中不符合上述条件的是( )
| A. | AlCl3 | B. | Na2O2 | C. | FeCl2 | D. | Al2S3 |
8.工业刻制印刷电路的主要原理为:Cu+2FeCl3=2FeCl2+CuCl2.有关该反应的说法正确的是( )
| A. | Cu是氧化剂 | B. | FeCl3是还原剂 | ||
| C. | Cu在反应中失去电子 | D. | FeCl3发生氧化反应 |