题目内容
5.下列物质中含氢原子数最多的是 ( )| A. | 2mol CH4 | B. | 3mol NH3 | C. | 4mol H2O | D. | 6mol HCl |
分析 根据物质组成知可以计算H原子物质的量,再结合N=nNA确定该元素原子个数多少,据此分析解答.
解答 解:A.根据甲烷分子构成知,2molCH4中n(H)=4n(CH4)=4×2mol=8mol;
B.根据氮气分子构成知,3mol NH3中n(H)=3n(NH3)=3mol×3=9mol;
C.根据水分子构成知,4mol H2O中n(H)=2n(H2O)=4mol×2=8mol;
D.根据HCl分子构成知,6molHCl中n(H)=n(HCl)=6mol,
再结合N=nNA知,n(H)越大H原子个数越多,所以H原子个数最多的是B,故选B.
点评 本题考查物质的量有关计算,明确同一物质中物质物质的量与元素物质的量关系是解本题关键,侧重考查分析计算能力,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
13.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 28g乙烯(C2H4)中含有的π键数与13g乙炔(C2H2)中含有的π键数一样多 | |
| B. | 通过MnO2催化使H2O2分解,产生16g O2时转移电子数为2NA | |
| C. | 2.24L NH3中含共价键数目一定为0.3NA | |
| D. | 5.6g Fe投入100mL 3.5mol•L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |
10.m g相对分子质量为M的二元强碱溶于水配制V L溶液,该溶液中c(OH-)为( )
| A. | $\frac{m}{MV}$mol•L-1 | B. | $\frac{2m}{MV}$mol•L-1 | C. | $\frac{m}{2MV}$mol•L-1 | D. | $\frac{2M}{mV}$mol•L-1 |
17.已知王水由盐酸和硝酸组成,c(Cl-)+c(NO3-)=18mol•L-1.为了测定王水的组成,取100mL该王水加水稀释至250mL,取25mL稀溶液加入足量的硝酸银溶液,过滤、洗涤、烘干、称重,得固体质量mg.则该王水中硝酸的物质的量浓度(mol•L-1)为( )
| A. | $\frac{10m}{143.5}$ | B. | $\frac{100m}{143.5}$ | C. | 18-$\frac{100m}{143.5}$ | D. | 18-$\frac{10m}{143.5}$ |
14.N的质量数为14,在微粒[NH3T]中,电子数、质子数、中子数之比为( )
| A. | 10:7:11 | B. | 10:11:9 | C. | 10:11:8 | D. | 11:9:10 |
15.含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中Cl-为1.5mol,K+为1.0mol,Na+为0.5mol,Mg2+为0.5mol,则SO42-的物质的量为( )
| A. | 0.15 mol | B. | 0.25 mol | C. | 0.5 mol | D. | 1 mol |
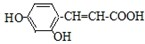 ;
;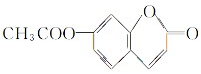 .
. ②
②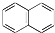 ③
③ ④
④ ⑤
⑤