题目内容
12.对于下列装置的分析不正确的是( )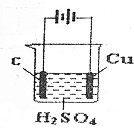
| A. | 这是一个电解池 | |
| B. | C作阴极,Cu作阳极 | |
| C. | 电解的过程实际上是电解水 | |
| D. | 石墨电极上的反应是4OH--4e-=O2↑+2H20 |
分析 A、有电源的装置属于电解池;
B、和电源的正极相连的是阳极,和电源的负极相连的是阴极;
C、根据放电顺序确定电解池的两极反应,进而确定总反应;
D、在电解池的阳极上发生失电子的氧化反应,据此回答.
解答 解:A、该装置是有电源的装置,属于电解池,故A正确;
B、C和电源的正极相连的是阳极,Cu和电源的负极相连的是阴极,故B错误;
C、根据放电顺序,在阳极上是氢氧根离子失电子的反应,在阴极上是氢离子得电子的还原反应过程,电解的实质是电解水,故C正确;
D、石墨电极和电源的正极相连,是阳极,在电解池的阳极上发生失电子的氧化反应,即4OH--4e-=O2↑+2H20,故D正确.
故选B.
点评 本题考查学生电解池的工作原理以及电极反应式的书写,注意知识的归纳和梳理是解题的关键,难度中等.

练习册系列答案
相关题目
2.关于药品的下列说法中错误的是( )
| A. | 氢氧化钠、氢氧化铜、氢氧化铁等物质都可作抗酸药 | |
| B. | 毒品是指由于非医疗目的而反复使用使人产生成瘾性的药品,如吗啡、冰毒等 | |
| C. | 禁止运动员在体育比赛中服用麻黄碱 | |
| D. | 用青霉素前使用者一定要进行皮肤敏感试验 |
3.下列叙述正确的是( )
| A. | 12g金刚石中含有C-C键4NA | |
| B. | 基态氧原子的电子排布图: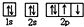 | |
| C. | H2SO4、H3PO4、HClO4的酸性依次减弱 | |
| D. | 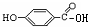 的沸点比 的沸点比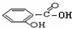 的沸点高 的沸点高 |
20.用相对分子质量为43的烷基取代丁烷分子中的一个氢原子,所得有机产物的结构有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.以下六种含铁元素的纯净晶体①Fe②FeO③Fe2O3④Fe3O4⑤FeS⑥FeS2,其中颜色不是黑色的是( )
| A. | ①②④ | B. | ①③⑤ | C. | ①③⑥ | D. | ③⑤⑥ |
1.在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:A(g)?B(g)+C(g)△H=+85.1kJ•mol-1,反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为升高温度、降低压强.
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为$\frac{P-P{\;}_{0}}{P{\;}_{0}}$×100%.平衡时A的转化率为94.1%,列式并计算反应的平衡常数K1.5mol/L.
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=$\frac{0.10P}{P{\;}_{0}}$mol,n(A)=0.10×(2-$\frac{p}{p{\;}_{0}}$)mol.
②下表为反应物A浓度与反应时间的数据,计算a=0.051;.
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是每隔4h,A的浓度减小一半,由此规律推出反应在12h时反应物的浓度c(A)为0.013mol•L-1.
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
(1)欲提高A的平衡转化率,应采取的措施为升高温度、降低压强.
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为$\frac{P-P{\;}_{0}}{P{\;}_{0}}$×100%.平衡时A的转化率为94.1%,列式并计算反应的平衡常数K1.5mol/L.
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=$\frac{0.10P}{P{\;}_{0}}$mol,n(A)=0.10×(2-$\frac{p}{p{\;}_{0}}$)mol.
②下表为反应物A浓度与反应时间的数据,计算a=0.051;.
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol•L-1) | 0.10 | a | 0.026 | 0.0065 |
 在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol•L-1和b mol•L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图所示.
在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol•L-1和b mol•L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图所示.