题目内容
【题目】下列叙述不正确的是![]()
A.金刚石、SiC、NaF、NaCl、![]() 、
、![]() 晶体的熔点依次降低
晶体的熔点依次降低
B.CaO晶体结构与NaCl晶体结构相似,CaO晶体中![]() 的配位数为6,且这些最邻近的
的配位数为6,且这些最邻近的![]() 围成正八面体
围成正八面体
C.设NaCl的摩尔质量为![]() ,NaCl的密度为
,NaCl的密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]()
![]() ,在NaCl晶体中,两个距离最近的
,在NaCl晶体中,两个距离最近的![]() 中心间的距离为
中心间的距离为
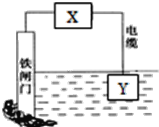
D.X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的化学式为![]()
【答案】D
【解析】
A. 金刚石、SiC属于原子晶体,键长![]() ,故金刚石中化学键更稳定,其熔点更高,NaF、NaCl都属于离子晶体,氟离子半径小于氯离子比较,故NaF的晶格能大于NaCl,则NaF的熔点更高,H2O、H2S都属于分子晶体,水分子之间存在氢键,熔点较高,熔点原子晶体
,故金刚石中化学键更稳定,其熔点更高,NaF、NaCl都属于离子晶体,氟离子半径小于氯离子比较,故NaF的晶格能大于NaCl,则NaF的熔点更高,H2O、H2S都属于分子晶体,水分子之间存在氢键,熔点较高,熔点原子晶体![]() 离子晶体
离子晶体![]() 分子晶体,故金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低,故A正确;
分子晶体,故金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低,故A正确;
B. CaO晶体结构与NaCl晶体结构相似,氯化钠的晶胞图为 ,若Ca2+处于体心、棱中间,O2-位于面心、顶点,晶体中体心Ca2+与面心的6个O2-距离最近,Ca2+配位数为6,且这些最邻近的O2-围成正八面体,故B正确;
,若Ca2+处于体心、棱中间,O2-位于面心、顶点,晶体中体心Ca2+与面心的6个O2-距离最近,Ca2+配位数为6,且这些最邻近的O2-围成正八面体,故B正确;
C. 氯化钠的晶胞图为 ,假设绿色球为Cl-,处于面对角线上的Cl-之间距离最近,设二者距离为
,假设绿色球为Cl-,处于面对角线上的Cl-之间距离最近,设二者距离为![]() ,则晶胞棱长
,则晶胞棱长![]() ,晶胞体积
,晶胞体积![]() ,晶胞中Cl-数目
,晶胞中Cl-数目![]() ,晶胞中Na+数目也是4,晶胞质量
,晶胞中Na+数目也是4,晶胞质量![]() ,解得
,解得![]()
 ,故C正确;
,故C正确;
D.处于棱的中心的原子为4个晶胞共用,位于顶角的原子为8个晶胞共用,晶胞中X数目![]() ,Y数目
,Y数目![]() ,则该晶体的组成式为
,则该晶体的组成式为![]() ,故D错误,
,故D错误,
答案选D。

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案【题目】4种相邻的主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
m | n | ||
x | y |
(1)元素x在周期表中的位置是第____。其单质可采用电解熔融的___方法制备。用电子式表示该化合物的形成过程:___。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是____,碱性最强的是____。(填化学式)
(3)气体分子(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是____。