题目内容
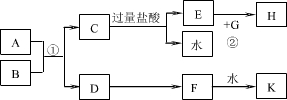
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.请回答下列问题:
(1)红褐色胶体粒子直径大小的范围:
(2)B的化学式:
(3)①写出C的溶液(A→C稀硫酸过量)与双氧水反应的离子方程式:
②写出B与少量稀硝酸反应的离子反应方程式:
③写出A的三价氯化物水溶液与NaHCO3溶液混合后反应的离子方程式:
(4)写出鉴定E中阳离子的实验方法和现象:
(1)红褐色液体是氢氧化铁胶体,分散质粒子直径大小的范围是1nm-100nm,
故答案为:1nm-100nm;
(2)依据推断可知B的化学式为:FeS,
故答案为:FeS;
(3)①①FeSO4的溶液(A→C稀硫酸过量)与双氧水在酸性溶液中反应,亚铁离子被过氧化氢氧化为三价铁,过氧化氢被还原为水,离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
②FeS与少量稀硝酸反应被氧化为硫单质,离子反应方程式:3FeS+8H++2NO3-═3 Fe2++3S↓+2NO↑+4H2O,
故答案为:3FeS+8H++2NO3-═3Fe2++3S↓+2NO↑+4H2O;
③铁的三价氯化物水溶液与NaHCO3溶液混合后反应的离子方程式:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑,
故答案为:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑;
(4)E中有铵根离子,可取少量E于试管中,用胶头滴管加入溶液,加热试管,可观察到试管口处湿润的红色石蕊试纸变蓝,说明有铵根离子,
故答案为:取少量E于试管中,用胶头滴管加入溶液,加热试管,可观察到试管口处湿润的红色石蕊试纸变蓝.

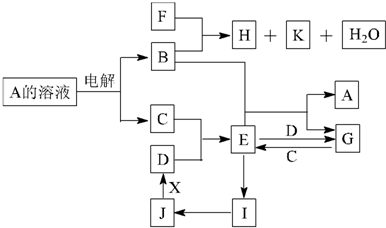
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
 |
已知:A、B、C、D、E是单质,组成它们的元素的原子序数依次为a、b、c、d、e;且3(a + b) = 2(a + c) = 3(d -a),X、Y、Z、M、N、W、H、K是化合物,其中X是B和C的化合产物的水溶液。请回答下列问题:
(1)用电子式表示X中溶质的形成过程:_______________,组成C的元素的原子结构示意图是_____ 。
(2)写出B在氧气中燃烧生成的产物与H2O反应的化学方程式:_______________。
(3)组成单质B、C、D的三种元素简单离子的离子半径由大到小的顺序是__ _(用离子符号表示)。
(4)写出K与过量的氨水反应的化学方程式 ;写出M在水溶液中电离的方程式 。
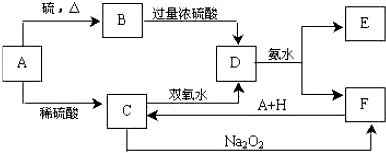
中学化学中几种常见物质的转化关系如下图所示(部分反应物、生成物及反应条件已略去):
已知:B、C、D为常见单质,其中C为气体,B、D为金属;F为常见的强酸;K常温下为气体,目能使品红溶液褪色;将 E 溶液滴入沸水可制得一种红褐色胶体; J 为红棕色固体。请回答下列问题:
 |
( l ) B 的化学式为 ;
写出 B 与 F 反应的化学方程式
( 2)实验中保存 G 溶液时要加入 目的是
( 3)为实现J一D的变化,若X是非金属单质,则X可能是 (写化学式); 若X是金属单质,请写出 J 一 D 反应的化学方程式