题目内容
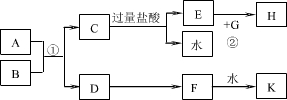
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
 |
已知:A、B、C、D、E是单质,组成它们的元素的原子序数依次为a、b、c、d、e;且3(a + b) = 2(a + c) = 3(d -a),X、Y、Z、M、N、W、H、K是化合物,其中X是B和C的化合产物的水溶液。请回答下列问题:
(1)用电子式表示X中溶质的形成过程:_______________,组成C的元素的原子结构示意图是_____ 。
(2)写出B在氧气中燃烧生成的产物与H2O反应的化学方程式:_______________。
(3)组成单质B、C、D的三种元素简单离子的离子半径由大到小的顺序是__ _(用离子符号表示)。
(4)写出K与过量的氨水反应的化学方程式 ;写出M在水溶液中电离的方程式 。
(1)

(2)2Na2O2 + 2H2O === 4NaOH + O2↑(3)Cl-> Na+ > Al3+ (4)AlCl3+3NH3??H2O=Al(OH)3↓+3NH4Cl;AlO-+H++H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH-
Al3++3OH-
解析:
中学电解氯化钠、氯化钾水溶液都生成三种物质:氯气、氢气和碱;因A、C为单质,故Y为碱,碱溶液与单质反应产生单质A,推知:A为氢气,C为氯气,Y为硅或铝,又因为Z和K都含有组成D的元素,且二者混合生成M,说明D为铝,Z为偏铝酸钠,W为氯化氢,K为氯化铝,M为氢氧化铝。E与盐酸反应生成氢气,说明E为金属,由N与H之间转化关系知,E为铁,N为氯化铁,H为氯化亚铁。根据推知的元素原子序数,a=1,c=17,d=13,e=26,由3(a+b)=2(a+c)得,b=11,即B单质的组成元素为钠。
X为氯化钠,它是离子化合物,形成过程为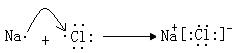 (2)钠在氧气中燃烧生成过氧化钠;(3)Na+,Al3+离子的电子数都是10,质子数越大,半径越小,离子半径:Na+>Al3+,Cl-有三个电子层,半径最大:即Cl->Na+>Al3+.
(2)钠在氧气中燃烧生成过氧化钠;(3)Na+,Al3+离子的电子数都是10,质子数越大,半径越小,离子半径:Na+>Al3+,Cl-有三个电子层,半径最大:即Cl->Na+>Al3+.

 寒假天地重庆出版社系列答案
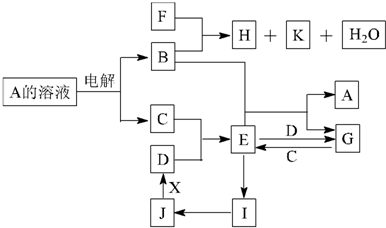
寒假天地重庆出版社系列答案中学化学中几种常见物质的转化关系如下图所示(部分反应物、生成物及反应条件已略去):
已知:B、C、D为常见单质,其中C为气体,B、D为金属;F为常见的强酸;K常温下为气体,目能使品红溶液褪色;将 E 溶液滴入沸水可制得一种红褐色胶体; J 为红棕色固体。请回答下列问题:
 |
( l ) B 的化学式为 ;
写出 B 与 F 反应的化学方程式
( 2)实验中保存 G 溶液时要加入 目的是
( 3)为实现J一D的变化,若X是非金属单质,则X可能是 (写化学式); 若X是金属单质,请写出 J 一 D 反应的化学方程式