��Ŀ����
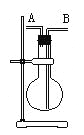
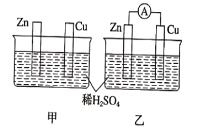
����Ŀ���ֱ���ͼ�ס�����ʾװ�ý���ʵ�飬ͼ�������ձ������Һ��Ϊ2LͬŨ�ȵ�ϡ���ᣬ����AΪ����������ش��������⣺
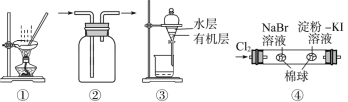
(1)���������У���ȷ����_______(����ĸ)
A������Һ��H+����пƬ�ƶ�
B�����ձ���пƬ����������ݲ���
C�����ձ�����ҺpH������
D������пƬ�Ǹ���������ͭƬ������
E���ҵ��ڵ�·�е�������Zn����Һ��Cu
(2)ʵ��ʱ���ס���ͬʱ��ʼ��Ӧ��0��15�����ڣ���ü���пƬ����������19.5�ˣ������ռ�������13.44��(��ת��Ϊ��״��)����������Ũ�ȵı仯��ʾ������װ�õķ�Ӧ���ʷֱ�Ϊ��v(��)��_________ mol��L��1��min��1��v(��)��_________ mol��L��1��min��1��v(��)___v(��)(������� =)����Ҫԭ����__________��
(3)�仯����������ת������Ҫ��ʽ����Ϊ _________����Ϊ____________��
(4)����ʵ���У���������ỻ����������Һ����д��ͭ�缫�ĵ缫��Ӧ����ʽ��_______����ʱ��װ����������������____________��
���𰸡�ACE 0.01 0.02 �� ��װ���γ���ԭ��أ��ӿ��˷�Ӧ���� ��ѧ��ת��Ϊ���� ��ѧ��ת��Ϊ���� Ag����e��=Ag ͭƬ����������ɫ��������
��������
��װ���У�пƬ��ͭƬû��ͨ�����������������γ�ԭ��أ�Zn��ϡ����ֱ�ӷ�Ӧ����������п��������������ѧ��ʴ������ѧ��ת��Ϊ���ܣ�����пƬ���������ݳ���ͭ��ϡ�����Ӧ��û������������װ���У�ZnƬ��ͭƬ�õ������ӣ�����ϡ������Һ�У��Ӷ��γ�ԭ��أ�пƬ��������ͭƬ��������пƬ�����ܽ⣬ͭƬ�ϲ����������ݳ���������ָ��ƫת����װ�ý���ѧ��ת��Ϊ���ܡ�
(1)A������Һ�У�п��ϡ����ֱ�ӷ�Ӧ������пʧȥ�ĵ��Ӹ�����пƬ���棬����H+����пƬ�ƶ���A��ȷ��
B�������У�H+��ͭƬ����õ��ӣ�����пƬ����û�����ݲ�����B����ȷ��
C�����ձ��о�����H+����ҺpH������C��ȷ��
D�����в����γ�ԭ��أ�����пƬ�����缫��D����ȷ��
E������Zn�缫Ϊ������CuΪ���������Ե�������Zn����Һ��Cu��E��ȷ��
��ѡACE����Ϊ��ACE��
(2)ʵ��ʱ���ס���ͬʱ��ʼ��Ӧ��0��15�����ڣ���ü���пƬ����������19.5�ˣ������ռ�������13.44��(��ת��Ϊ��״��)����������Ũ�ȵı仯��ʾ������װ�õķ�Ӧ���ʷֱ�Ϊ��v(��)��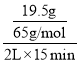 =0.01mol��L��1��min��1��v(��)��
=0.01mol��L��1��min��1��v(��)�� =0.02mol��L��1��min��1��v(��)��v(��)����Ҫԭ������װ���γ���ԭ��أ��ӿ��˷�Ӧ���ʡ���Ϊ��0.01��0.02��������װ���γ���ԭ��أ��ӿ��˷�Ӧ���ʣ�
=0.02mol��L��1��min��1��v(��)��v(��)����Ҫԭ������װ���γ���ԭ��أ��ӿ��˷�Ӧ���ʡ���Ϊ��0.01��0.02��������װ���γ���ԭ��أ��ӿ��˷�Ӧ���ʣ�
(3)�����Ϸ���֪���仯����������ת������Ҫ��ʽ����Ϊ��ѧ��ת��Ϊ���ܣ���Ϊ��ѧ��ת��Ϊ���ܡ���Ϊ����ѧ��ת��Ϊ���ܣ���ѧ��ת��Ϊ���ܣ�
(4)����ʵ���У���������ỻ����������Һ����ͭ�缫��Ag+�õ�������Ag���缫��Ӧ����ʽ��Ag����e��=Ag����ʱ��װ����������������Ag(����ɫ)��������ͭƬ����������ɫ������������Ϊ��Ag����e��=Ag��ͭƬ����������ɫ����������

����Ŀ����Դ�����ͬ��ע����Ҫ���⣬������һ�ֽྻ����Դ��
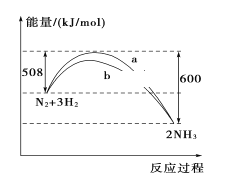
(1)���鲻��������ȼ�ϣ��������������ϳ���(CO��H2)��CH4��H2O(g)ͨ��۽�̫���ܷ�Ӧ����������ӦCH4(g)+H2O(g)=CO(g)+3H2(g)��H1����֪ijЩ��ѧ���ļ����������±���
��ѧ�� | C��H | H��H | C��O | O��H |
����/kJ��mol��1 | 413 | 436 | 1076 | 463 |
���H1=___________kJ��mol��1
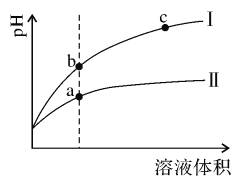
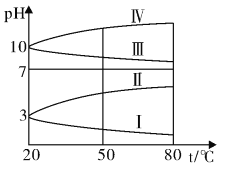
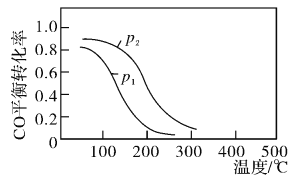
(2)�úϳ������ɼ״��ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g)��H2����2L�����ܱ������У������ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3OH(g)��H2����2L�����ܱ������У������ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
200��ʱn(H2)��ʱ��ı仯���±���ʾ
t/min | 0 | 1 | 2 | 3 |
n(H2)/mol | 6.0 | 3.4 | 2.0 | 2.0 |
�١�H2___________0(�>����<����=��)
������˵����ȷ����___________(����ĸ���)��
a.��ƽ����������г���ϡ�����壬ѹǿ����ƽ��������Ӧ�����ƶ�
b.�����¶ȣ��÷�Ӧ��ƽ�ⳣ�����
C.�����������ܶȲ��䣬��Ӧ�ﵽ�����
d.ͼ��ѹǿp1>p2
��200��ʱ���÷�Ӧ��ƽ�ⳣ��K=___________��
(3)���顢������KOH��Һ�����ȼ�ϵ�ء����ȼ�ϵ�ع���ʱ��ͨ�����ĵ缫Ϊ___________������缫��ӦʽΪ______________________��ͨ�������ĵ缫��ӦʽΪ��___________��