题目内容
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
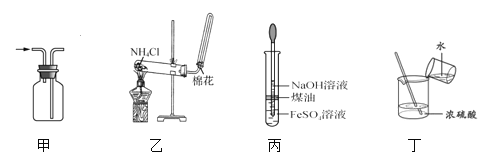
A. 用图甲所示装置收集 NO B. 用图乙所示装置制备 NH3
C. 用图丙所示装置制备 Fe(OH)2 D. 用图丁所示装置稀释浓 H2SO4
【答案】C
【解析】
A、NO能与氧气反应生成二氧化氮,不能用排空气法收集,选项A错误;
B、用图乙所示装置制备 NH3,氯化铵受热分解产生的氨气和氯化氢在试管口又反应生成氯化铵固体,无法得到氨气,选项B错误;
C、Fe(OH)2白色沉淀极易被空气中的氧气氧化:4 Fe(OH)2+2H2O+O2═4 Fe(OH)3,生成红褐色沉淀,所以制备Fe(OH)2沉淀需隔绝空气,煤油的密度比水小,浮在上面,能起到隔绝空气的作用,所以该装置能实现制备Fe(OH)2沉淀,选项C正确;
D、稀释浓 H2SO4时应将浓硫酸慢慢注入水中并不断搅拌,而不能将水倒入浓硫酸中,选项D错误;
答案选C。

练习册系列答案
相关题目