题目内容
【题目】煤的气化是高效、清洁的利用煤炭的重要途径之一。
(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法。已知:
① C(s)+ O2 (g) = CO2 (g) ΔH = -393.5 kJ·mol-1
② CO(g) + ![]() O2 (g) = CO2 (g) ΔH = -283.0 kJ·mol-1
O2 (g) = CO2 (g) ΔH = -283.0 kJ·mol-1
③ H2(g) + ![]() O2 (g) = H2O (g) ΔH = -241.8 kJ·mol-1
O2 (g) = H2O (g) ΔH = -241.8 kJ·mol-1
则碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是 ,该反应的化学平衡常数K随温度的升高将 (填“增大”、“减小”或“不变”)。
(2)CO可以与H2O(g)进一步发生反应CO(g) + H2O(g)![]() CO2(g)+H2(g) ΔH<0。在甲、乙两个恒容密闭容器中,起始时按照下表数据进行投料,在800℃时达到平衡状态,K=1.0。
CO2(g)+H2(g) ΔH<0。在甲、乙两个恒容密闭容器中,起始时按照下表数据进行投料,在800℃时达到平衡状态,K=1.0。
H2O | CO | CO2 | H2 | |
甲 n/ mol | 0.10 | 0.30 | 0.10 | 0.50 |
乙 n/ mol | 0.20 | 0.20 | 0 | 0 |
起始时,甲容器中反应向 (填“正反应”或“逆反应”)方向进行;平衡时,乙容器中CO的转化率为 。

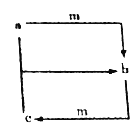
②右图表示上述反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况。则t2时刻发生改变的所有可能的条件是 。
(3)以CO为燃料制作燃料电池,电池的正极入O2和CO2,负极通入CO,电解质是熔融碳酸钠,工作时负极反应式为 ,若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为(标准状况下) L。
【答案】(1)C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol(2分),增大(2分)
(2)①逆反应(2分);50%(2分)②降低温度、增加水蒸气浓度或减小氢气浓度.(2分)
(3)CO+CO32-=2CO2+2e- (2分) 6.72(2分)
【解析】
试题分析:(1)已知:① C(s)+ O2 (g) = CO2 (g) ΔH = -393.5 kJ·mol-1
② CO(g) + ![]() O2 (g) = CO2 (g) ΔH = -283.0 kJ·mol-1
O2 (g) = CO2 (g) ΔH = -283.0 kJ·mol-1
③ H2(g) + ![]() O2 (g) = H2O (g) ΔH = -241.8 kJ·mol-1
O2 (g) = H2O (g) ΔH = -241.8 kJ·mol-1
则根据盖斯定律可知①-②-③即得到碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol;正反应是吸热反应,升高温度平衡向正反应方向进行,因此该反应的化学平衡常数K随温度的升高将增大。
(2)①起始时,甲容器中浓度熵=![]() >1,所以反应向逆反应方向进行;平衡时,乙容器中消耗CO的物质的量是x,由于反应前后体积不变,因此用物质的量代替浓度计算平衡常数,则
>1,所以反应向逆反应方向进行;平衡时,乙容器中消耗CO的物质的量是x,由于反应前后体积不变,因此用物质的量代替浓度计算平衡常数,则![]() ,解得x=0.1,所以CO的转化率为50%。
,解得x=0.1,所以CO的转化率为50%。
②t2时CO2浓度逐渐增大,CO浓度逐渐减小,这是你平衡向正反应方向进行。由于正反应是体积不变的放热反应,因此改变的条件可能是降低温度、增加水蒸气浓度或减小氢气浓度;
(3)电解质是熔融碳酸钠,工作时负极通入CO,所以电极反应式为CO-2e-+CO32-=2CO2;若使用该电池电解熔融氧化铝制取10.8g铝,物质的量是10.8g÷27g/mol=0.4mol,注意1.2mol,所以根据电子得失守恒可知需要氧气是1.2mol÷4=0.3mol,在标准状况下的体积为0.3mol×22.4L/mol=6.72L。