题目内容
【题目】类推法在化学学习过程中广泛使用,如下四项推测,其中正确的是( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据结构和组成相似的物质,沸点随相对分子质量增大而升高,推出NH3的沸点低于PH3
C.CO2中的C采用sp杂化轨道成键,CS2中的C也是采用sp杂化轨道成键
D.CH4的空间结构为正四面体,键角为109°28′,P4的空间结构也为正四面体,键角为109°28′
【答案】C
【解析】
A.同周期元素第一电离能的变化趋势为:从左到右逐渐增大。但镁和铝例外,因为镁的价电子排布是3s2,s轨道全满,较稳定。而铝是3s23p1,不是全满、半满、全空中任意一种情况,稳定性较差,故铝的第一电离能比镁小,A错误;
B.氨分子间存在氢键,导致沸点升高,而PH3分子间没有氢键,所以NH3的沸点高于PH3, B错误;
C.CO2中C和O形成双键,结构式为O=C=O,空间构型为直线型;CS2中S和O也形成双键,结构式为S=C=S,空间构型为直线型,所以C和S均为sp杂化,C正确;
D.CH4的空间结构为正四面体,空间构型为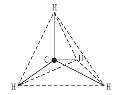 ,键角为109°28′;白磷的空间结构也为正四面体,空间构型为
,键角为109°28′;白磷的空间结构也为正四面体,空间构型为![]() ,键角为60°,D错误;
,键角为60°,D错误;
故选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目