题目内容
【题目】依据原子结构,元素周期表填空
(1)某元素的原子序数为33,该元素原子的价电子排布式为____________________________该元素原子核外______个能级,_______个原子轨道。
(2)铜原子核外电子排布式为_________________________,属于第_____周期,______族。
(3)位于第四周期ⅥB族元素核外电子排布式___________________________,价电子的排布图 ____________________。
(4)某元素原子的价电子构型为3d54s2,它属于____区元素,最高正化合价为____,元素符号是_____
【答案】4s24p3 8 8 1s22s22p63s23p63d104s1 4 IB 1s22s22p63s23p63d54s1 ![]() d +7 Mn
d +7 Mn
【解析】
(1)原子序数为33的元素为砷,它是主族元素,该元素原子的价电子排布式为4s24p3;该元素原子核外能级数为8;原子轨道数为8。答案为:4s24p3;8;8;
(2)铜原子核外电子排布式为1s22s22p63s23p63d104s1,周期数为4,族序数为ⅠB。答案为:1s22s22p63s23p63d104s1;4;ⅠB;
(3)位于第四周期ⅥB族元素,核外电子排布式1s22s22p63s23p63d54s1,价电子的排布图为![]() 。答案为:1s22s22p63s23p63d54s1;
。答案为:1s22s22p63s23p63d54s1;![]() ;
;
(4)某元素原子的价电子构型为3d54s2,它属于d区元素,最高正化合价为+7价,元素符号是Mn。答案为:d;+7;Mn。

 挑战100单元检测试卷系列答案
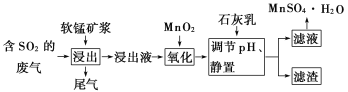
挑战100单元检测试卷系列答案【题目】软锰矿的主要成分是二氧化锰,用软锰矿浆吸收工业废气中的二氧化硫,可以制备高纯度的硫酸锰晶体,其流程如下图所示:
已知:
①浸出液中的金属阳离子主要是![]() ,还含有少量的
,还含有少量的![]() 、
、![]() 等,且
等,且![]() .
.
②几种离子开始沉淀和完全沉淀时的pH如表所示:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| 7.6 | 9.7 |
| 2.7 | 3.7 |
| 3.8 | 4.7 |
| 8.3 | 9.8 |
根据上述流程,回答下列问题:
(1)写出二氧化锰与二氧化硫反应的化学方程式:_____________.
(2)用离子方程式表示加入二氧化锰的作用:________________________________.
(3)从表中数据来看,________(填“能”或“不能”)取消“加入二氧化锰”的步骤,原因是________________________.
(4)下列试剂能替代二氧化锰的是________(填序号).
A.双氧水 B.氯水 C.高锰酸钾溶液 D.次氯酸钠
(5)有同学认为可以用碳酸锰![]() 或氢氧化锰
或氢氧化锰![]() 替代石灰乳,你是否同意此观点?简述理由:______________________________________________________.
替代石灰乳,你是否同意此观点?简述理由:______________________________________________________.
(6)从含硫酸锰的滤液中提取硫酸锰晶体的操作是_____________________________.