题目内容
【题目】已知:2CrO42-+2H+![]() Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )
Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )
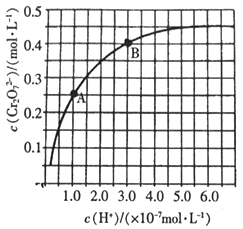
A. 平衡时,pH越小,c(Cr2O72-)越大
B. A、B两点c(CrO42-)之比为5:2
C. B点CrO42-的平衡转化率为40%
D. 平衡时,若溶液中c(CrO42-)=2c(Cr2O72-),则c(H+)=1.0×10-7mol·L-1
【答案】C
【解析】A、根据图像,c(H+)越大,c(Cr2O72-)越大,故A说法正确;B、A点c(Cr2O72-)=0.25mol·L-1,则c(CrO42-)=(1.0-0.25×2)mol·L-1=0.5mol·L-1,B点c(Cr2O72-)=0.4mol·L-1,则c(CrO42-)=(1.0-0.4×2)mol·L-1=0.2mol·L-1,因此两点c(CrO42-)的比值为0.5:0.2=5:2,故B说法正确;C、根据B选项分析,B点c(CrO42-)=0.2mol·L-1,则CrO42-的转化率为0.8/1.0×100%=80%,故C说法错误;D、令达到平衡时,c(Cr2O72-)=xmol·L-1,则c(CrO42-)=2xmol·L-1,根据铬元素守恒,2x+2x=1.0,解得x=0.25mol·L-1,根据图像,对应的c(H+)=1.0×10-7mol·L-1,故D说法正确。

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目