��Ŀ����
����Ŀ��ijС��̽����ϴ�Թܣ��ڱڸ����������ķ�Ӧԭ������������ʵ�顣
I.����̽��
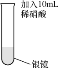
��1����ϡ������븽���������Թ��У���¼�������£�
ʵ��� | ʵ����� | ʵ������ |
| �����ϳ������ݣ���Һ���·�Ϊ��ɫ���壬���Թܿڸ���......���Թ��ڱ��ϵ������ܽ⡣ |
�ٲ�ȫ��Ӧ�е�ʵ������___��
��ʵ�����������ʧ������Ӧ�Ļ�ѧ����ʽΪ____��
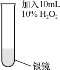
��2��Ϊ����ʵ����е����������Ⱦ����˫��ˮ��Һ���븽���������Թ��С�
ʵ��� | ʵ����� | ʵ������ |
| ���ҷ�Ӧ���д�����ɫ������������������ʹ�����ǵ�ľ����ȼ���Թ��ڱ��ϵ������ܽ⡣ |
���������Ʋ�H2O2��Ag����ΪAg+����ͨ��ʵ���ų������ֿ��ܡ���ʵ�鷽���ǣ��ڷ�Ӧ���Һ���У�����___��
�ڲ������Ϸ��֣���ʵ���������ܽ�����ղ���Ϊ������С��ֱ����1��100nm֮�䣩��Ag�����ɢ��Һ���У�������ʶ�𡣸�ͬѧͨ��ʵ��֤ʵ�����ֿ����ԡ����IJ����������ǣ�___��
��д����ʵ����з�����Ӧ�Ļ�ѧ����ʽ��___��
II.�������ϣ�����̽��
�������ף�Ag2O+4NH3H2O=2[Ag(NH3)2]++2OH-+3H2O
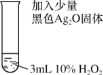
��3��̽��Ag2O��H2O2�ֽⷴӦ�е����ã���������ʵ�顣
ʵ��� | ʵ����� | ʵ������ |
| ���ҷ�Ӧ��������������ɫ���壬ͬʱ���Թܵײ�����������ɫ���� |
����ʵ����������룺Ag2O�ڷ�Ӧ����������������ʵ�飬��ʵ���Ӧ����Թ��м�����������Һx��������ʣ�ࡣ�ɴ���֤�˸ò������ȷ��
����ʵ���м�����������Һx��____��
��ʵ����з�����Ӧ�Ļ�ѧ����ʽΪ___��
���𰸡����ֺ���ɫ���� 3Ag+4HNO3=3AgNO3+NO��+2H2O ����ϡ����(��NaCl��Һ) ��һ��������Һ��a��������������� 2H2O2![]() O2��+2H2O ��ˮ H2O2+Ag2O=2Ag+O2��+H2O
O2��+2H2O ��ˮ H2O2+Ag2O=2Ag+O2��+H2O
��������
��1����ϡ������븽���������Թ��У��������ᷢ��������ԭ��Ӧ��3Ag+4HNO3=3AgNO3+NO��+2H2O��
��2���������ϡ����(��NaCl��Һ)����û�в�����ɫ������֤��������Ag+���ų���H2O2��Ag����ΪAg+�Ŀ��ܡ���a�д���ֱ����1~100nm��Ŀ��������ڽ��壬���ö����������飻
�۸���ʵ������������֪ʵ������ǹ��������������£������ֽ⣬��������������ѧ����ʽ��2H2O2![]() O2��+2H2O��
O2��+2H2O��
��3����������������ַ�Ӧ��õ������ʣ�����������ˮ���岻�ܽ⣬�����Ļ�ѧ����ʽΪH2O2+Ag2O=2Ag+O2��+H2O��
��1����ϡ������븽���������Թ��У��������ᷢ��������ԭ��Ӧ��3Ag+4HNO3=3AgNO3+NO��+2H2O�����������ϳ������ݣ���Һ���·�Ϊ��ɫ���壬���Թܿڸ������ֺ���ɫ���壻�Թ��ڱ��ϵ������ܽ⣬�ʱ����Ϊ�����ֺ���ɫ���壻3Ag+4HNO3=3AgNO3+NO��+2H2O��
��2�����ų�H2O2��Ag����ΪAg+�Ŀ��ܣ��������ϡ����(��NaCl��Һ)����û�в�����ɫ������֤��������Ag+���ų���H2O2��Ag����ΪAg+�Ŀ��ܣ��ʴ�Ϊ������ϡ����(��NaCl��Һ)��
��a�д���ֱ����1~100nm��Ŀ��������ڽ��壬���ö����������飬������һ��������Һ��a��������������ʴ�Ϊ����һ��������Һ��a���������������
�۸���ʵ������������֪ʵ������ǹ��������������£������ֽ⣬��������������ѧ����ʽ��2H2O2![]() O2��+2H2O���ʱ����Ϊ��2H2O2
O2��+2H2O���ʱ����Ϊ��2H2O2![]() O2��+2H2O��
O2��+2H2O��
��3������Ag2O������������ˮ�У�ת��Ϊ������Һ�����������ڰ�ˮ����������������ַ�Ӧ��õ������ʣ�����������ˮ���岻�ܽ⣬ʵ������ǹ��������������������Ӧ���������ʣ�����ˮ���仯ѧ����ʽΪH2O2+Ag2O=2Ag+O2��+H2O�������Ϊ���ٰ�ˮ����H2O2+Ag2O=2Ag+O2��+H2O��