题目内容
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。向甲、乙两个体积都为1.0L的恒容密闭容器中均充入2.0molNO2和1.0molO3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表。下列说法不正确的是( )
N2O5(g)+O2(g)。向甲、乙两个体积都为1.0L的恒容密闭容器中均充入2.0molNO2和1.0molO3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表。下列说法不正确的是( )

A.T1<T2
B.该反应△H<0
C.甲容器在温度为T1时的平衡常数为20mol·L-1
D.乙容器中,0~3s内的平均反应速率v(NO2)=0.2mol·L-1·s-1
【答案】A
【解析】
A.图表数据可知,甲容器中达到平衡时间短,反应的温度高T1>T2, A错误;
B.图表数据可知,甲容器中达到平衡时间短,反应的温度高,升温平衡向吸热反应方向进行,甲中平衡时氧气的物质的量小于乙容器,则该反应△H<0,B正确;
C.对于甲容器,发生反应2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应达到平衡时n(O2)=0.8 mol,n(N2O5)=n(O2)=0.8 mol,反应消耗n(O3)=0.8 mol,消耗n(NO2)=2×0.8 mol=1.6 mol,所以平衡时n(NO2)=2.0 mol-1.6 mol=0.4 mol,n(O3)=1.0 mol-0.8 mol=0.2 mol,反应容器的容积是1L,所以各种物质的平衡时的物质的量为物质的平衡浓度,则该反应的化学平衡常数K=
N2O5(g)+O2(g),反应达到平衡时n(O2)=0.8 mol,n(N2O5)=n(O2)=0.8 mol,反应消耗n(O3)=0.8 mol,消耗n(NO2)=2×0.8 mol=1.6 mol,所以平衡时n(NO2)=2.0 mol-1.6 mol=0.4 mol,n(O3)=1.0 mol-0.8 mol=0.2 mol,反应容器的容积是1L,所以各种物质的平衡时的物质的量为物质的平衡浓度,则该反应的化学平衡常数K=![]() =20,C正确;
=20,C正确;
D.乙容器中,0~3s内的平均反应速率v(NO2)=2v(O2)=2× =0.20 mol/(L·s),D正确;
=0.20 mol/(L·s),D正确;
答案选A。

 阅读快车系列答案
阅读快车系列答案【题目】将煤隔绝空气加强热(干馏)可得到焦炭、煤焦油、粗氨水和焦炉气。某焦炉气组成如下:
成分 | 氢气 | 甲烷 | 乙烯 | 丙烯 |
质量分数(%) | 20 | 56 | 14 | 10 |
将该焦炉气通过足量的溴水后,所得混合气体的平均相对分子质量约为
A.5.63B.7.02C.7.41D.10.12
【题目】(1)实验测得16 g甲醇CH3OH(l)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25 kJ的热量,试写出甲醇燃烧的热化学方程式: ____________________。
(2)合成氨反应N2(g)+3H2(g) ![]() 2NH3(g)ΔH=a kJ·mol-1,反应过程的能量变化如图所示:
2NH3(g)ΔH=a kJ·mol-1,反应过程的能量变化如图所示:
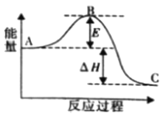
①该反应通常用铁作催化剂,加催化剂会使图中E______(填“变大”或“变小”),E的大小对该反应的反应热有无影响?______(填“有”或“无”)。
②有关键能数据如下:
化学键 | H—H | N—H | N≡N |
键能(kJ·mol-1) | 436 | 391 | 945 |
试根据表中所列键能数据计算a为____________。
(3)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:①N2(g)+2O2(g)=2NO2(g) △Η1=a kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △Η2=bkJ/mol
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_____________________。