题目内容
【题目】醋酸、氢硫酸、碳酸在常温下的电离常数如下表:

(1)能证明CH3COON是弱酸的事实是___。
A.CH3COOH易挥发
B.常温下,0.1mol·L-1CH3COONa溶液的pH大于7
C.醋酸不易腐蚀衣服
D.pH=3的CH3COOH溶液稀释10倍,溶液pH<4
E.等体积等浓度的CH3COOH溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
F.将一定量的CH3COOH溶液加入Na2CO3溶液中,有气泡产生
(2)煤的气化过程中产生的H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为___。
(3)t℃时,0.0lmol·L-1NaOH溶液的pH=11,则该温度下,水的离子积Kw=___mol2·L-2;该温度下,将pH之和为13的NaOH溶液和CH3COOH溶液等体积混合,所得溶液呈___(填“酸”、“碱”或“中”)性。
(4)在室温下,用蒸馏水稀释0.0lmol·L-1CH3COOH溶液,下列各项呈减小趋势的是___。
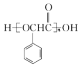
A.![]()
B.![]()
C.溶液中c(H+)和c(OH-)的乘积
D.溶液导电性
E.水的电离程度
(5)25℃时,向1m30.1mol·L-1H2S溶液(pH=4)中加入FeSO4·7H2O晶体,当开始生成沉淀时,加入FeSO4·7H2O晶体的质量为___g。
[已知:Ksp(FeS)=6.3×10-18mol-1·L-2,忽略混合过程中的体积变化]
【答案】BD H2S+CO32-=HS-+HCO3- 1.0×10-13mol2·L-2 酸 BD 250.2
【解析】
(1)(1)A.CH3COOH易挥发,挥发性不能判断酸性强弱。
B.常温下,0.1mol·L-1CH3COONa溶液的pH大于7,CH3COONa为强碱弱酸盐水解成碱性,可以判断CH3COOH是弱酸。
C.醋酸不易腐蚀衣服属于腐蚀性强弱不属于酸性。
D.pH=3的CH3COOH溶液稀释10倍,溶液pH<4,说明醋酸部分电离可以证明CH3COOH是弱酸。
E.等体积等浓度的CH3COOH溶液和盐酸,分别与足量镁粉反应,产生氢气一样多,属酸的通性不可以证明CH3COOH是弱酸。
F.将一定量的CH3COOH溶液加入Na2CO3溶液中,有气泡产生属酸的通性不可以证明CH3COOH是弱酸。
答案选 BD 。
(2)H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为H2S+CO32-=HS-+HCO3-。
(3)0.01mol/l的NaOH溶液中c(OH-)=0.01mol/L=10-2mol/L,pH为11的氢氧化钠溶液中c(H+)=10-11mol/L,该温度下水的离子积常数Kw=c(H+)·c(OH-)=10-11mol/L×10-2mol/L=10-13(mol/L)2。该温度下,pH之和为13的NaOH溶液和CH3COOH溶液等体积混合,由于醋酸的浓度大于氢氧化钠,醋酸过量,所得溶液呈酸性
(4)A.用蒸馏水稀释0.0lmol·L-1CH3COOH溶液,氢离子浓度增大的程度大于醋酸根,则![]() 增大。
增大。
B. ![]() =Kh/c(OH-),用蒸馏水稀释0.0lmol·L-1CH3COOH溶液c(OH-)增大,
=Kh/c(OH-),用蒸馏水稀释0.0lmol·L-1CH3COOH溶液c(OH-)增大,![]() 减小。
减小。
C. 溶液中c(H+)和c(OH-)的乘积等于水的电离平衡常数,水的电离平衡常数只与温度有关,用蒸馏水稀释0.0lmol·L-1CH3COOH溶液时不变。
D. 用蒸馏水稀释0.0lmol·L-1CH3COOH溶液时氢离子浓度下降,溶液导电性变弱。
E. 用蒸馏水稀释0.0lmol·L-1CH3COOH溶液时水的电离抑制变弱,水的电离程度变大。
答案选BD。
(5)25℃时,根据H2S电离平衡常数可知1m30.1mol·L-1H2S溶液(pH=4)中n(s2-)=![]() =7×10-15mol·L-1,根据Ksp(FeS)=6.3×10-18mol-1·L-2可知c(Fe2+)=9×10-4mol·L-1,所以 FeSO4·7H2O物质的量是0.9mol,质量为 250.2g。
=7×10-15mol·L-1,根据Ksp(FeS)=6.3×10-18mol-1·L-2可知c(Fe2+)=9×10-4mol·L-1,所以 FeSO4·7H2O物质的量是0.9mol,质量为 250.2g。

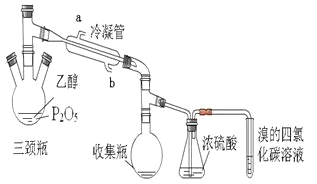
【题目】有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验。按右表所示的量和反应条件在三颈瓶中加入一定量P2O5,并注入95%的乙醇,并加热,观察现象。
实验 | P2O5 | 95%乙醇量 | 加热方式 |
实验1 | 2g | 4mL | 酒精灯 |
实验2 | 2g | 4mL | 水浴70℃ |
实验结果如下:
实验 | 实验现象 | ||
三颈瓶 | 收集瓶 | 试管 | |
实验1 | 酒精加入时,立刻放出大量的白雾,开始有气泡产生,当用酒精灯加热时,气泡加快生成并沸腾,生成粘稠状液体。 | 有无色液体 | 溶液褪色 |
实验2 | 酒精加入时,有少量白雾生成,当用水浴加热时,不产生气泡,反应一个小时,反应瓶内生成粘稠状液体 | 有无色液体 | 溶液不褪色 |
根据上述资料,完成下列填空。
(1)写出乙醇制乙烯的化学方程式______________________________________。
(2)上图装置中冷凝管的作用是___________,进水口为(填“a”或“b”)______,浓硫酸的作用是_____________。
(3)实验1使溴的四氯化碳溶液褪色的物质是___________。
(4)实验2中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外)。
(5)三颈瓶、收集瓶中的液体经检验为磷酸三乙酯,写出三颈瓶中生成磷酸的化学方程式
_____________________,P2O5在实验1中的作用是______________________ 。
(6)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是____________
②P2O5与95%乙醇在加热条件下可以发生的有机反应的类型是________反应。