题目内容
15.写出下列有机物的系统命名或结构简式:(1)
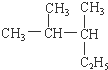 2,3-二甲基戊烷
2,3-二甲基戊烷(2)CH3CH(CH3)C(CH3)2(CH2)2CH32,3,3-三甲基己烷
(3)间甲基苯乙炔

(4)2-甲基-1,3-丁二烯.CH2=C(CH3)-CH=CH2.
分析 (1)(2)烷烃命名遵循“长、多、近、小、简”;
(3)芳香烃有2个取代基时,利用传统命名法可以命名为邻间对;
(4)二烯的命名选取含有2个双键的最长碳链.
解答 解:(1) 是烷烃,选取最长碳原子的为主链,主链含有5个,从离甲基最近的一端编号,写出名称为:2,3-二甲基戊烷,
是烷烃,选取最长碳原子的为主链,主链含有5个,从离甲基最近的一端编号,写出名称为:2,3-二甲基戊烷,
故答案为:2,3-二甲基戊烷;
(2)CH3CH(CH3)C(CH3)2(CH2)2CH3最长碳链为6,为己烷,在2、3号碳上分别含有1个和2个甲基,正确命名为:2,3,3-三甲基己烷,故答案为:2,3,3-三甲基己烷;
(3)间甲基苯乙炔的结构简式为: ,故答案为:
,故答案为: ;
;
(4)2-甲基-1,3-丁二烯,主链为1,3-丁二烯,在2号C含有1个甲基,该有机物的结构简式为:CH2=C(CH3)-CH=CH2,故答案为:CH2=C(CH3)-CH=CH2.
点评 本题考查了有机物的命名,题目难度不大,一般要求了解烷烃的命名、烯烃的命名、芳香烃的命名,难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
4.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加.相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E在周期表中位于第四周期第IB族,C基态原子核外电子排布式是1s22s22p63s1.
(2)A、B、D三种元素电负性由大到小排列顺序为N>C>Si,其中A的最高价氯化物为非极性分子.(填“极性分子”或“非极性分子”)
(3)A和B的最简单氢化物中沸点较高的NH3.原因是NH3分子间存在氢键.
(4)已知:
①AH4(g)+2BO2(g)=B2(g)+AO2(g)+2H2O(g) H1=-867kJ•mol-1
②2BO2(g)=B2 O4(g) H2=-56.9kJ•mol-1
写出AH4和B2O4反应的热化学方程式CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
| A | A的一种单质在自然界中硬度最大 |
| B | B元素的第一电离能比同周期相邻两个元素都大 |
| C | 同周期中,C元素的最高价氧化物对应的水化物的碱性最强 |
| D | D的基态原子M层电子数是K层的2 倍 |
| E | E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
(2)A、B、D三种元素电负性由大到小排列顺序为N>C>Si,其中A的最高价氯化物为非极性分子.(填“极性分子”或“非极性分子”)
(3)A和B的最简单氢化物中沸点较高的NH3.原因是NH3分子间存在氢键.
(4)已知:
①AH4(g)+2BO2(g)=B2(g)+AO2(g)+2H2O(g) H1=-867kJ•mol-1
②2BO2(g)=B2 O4(g) H2=-56.9kJ•mol-1
写出AH4和B2O4反应的热化学方程式CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
6.工业上由焦炭或天然气制氢气的过程中会产生一氧化碳.为了除去氢气中混有的一氧化碳,可在催化剂存在的条件下发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ/mol
该反应在工业上被称为“一氧化碳变换”反应.
(1)在一个容积为1L的密闭容器中加入1molCO和3molH2O(g),发生上述反应,5min后达到平衡,测得该反应实际放出的热量为20.5kJ,迅速导出热量,保持容器中温度不变.则该时间范围内反应的平均速率ν(CO)=0.1mol/(L•min);平衡常数K的数值为0.2.
(2)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数).
现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,将其中的CO除去.已知不同温度
及反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)下,变换反应后平衡混合气体中CO的体积分数如下表所示:
①平衡混合气体中CO的体积分数越大,则CO的平衡转化率越小(填“大”或“小”).
②从该反应的化学方程式分析,反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)越大,CO的平衡转化率越大(填
“大”或“小”),与上表中的数据分析结果相符(填“相符”或“不符”).根据对上表的分析,为提高CO平衡转化率,还可以采取的措施是降低温度.
③不同温度下该反应K值:K(300℃)<K(200℃)(填“>”、“=”或“<”).
④温度是一氧化碳变换工艺中最重要的条件,实际生产过程中将温度控制在300℃左右,其原因是升高温度,会提高反应速率,但平衡逆向移动,CO的平衡转化率下降,实际生产中应综合考虑速率和平衡两个方面.
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ/mol
该反应在工业上被称为“一氧化碳变换”反应.
(1)在一个容积为1L的密闭容器中加入1molCO和3molH2O(g),发生上述反应,5min后达到平衡,测得该反应实际放出的热量为20.5kJ,迅速导出热量,保持容器中温度不变.则该时间范围内反应的平均速率ν(CO)=0.1mol/(L•min);平衡常数K的数值为0.2.
(2)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数).
现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,将其中的CO除去.已知不同温度
及反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)下,变换反应后平衡混合气体中CO的体积分数如下表所示:
| 温度/℃\CO的体积分数%\投料比 | $\frac{n({H}_{2}O)}{n(CO)}$=1 | $\frac{n({H}_{2}O)}{n(CO)}$=3 | $\frac{n({H}_{2}O)}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
②从该反应的化学方程式分析,反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)越大,CO的平衡转化率越大(填
“大”或“小”),与上表中的数据分析结果相符(填“相符”或“不符”).根据对上表的分析,为提高CO平衡转化率,还可以采取的措施是降低温度.
③不同温度下该反应K值:K(300℃)<K(200℃)(填“>”、“=”或“<”).
④温度是一氧化碳变换工艺中最重要的条件,实际生产过程中将温度控制在300℃左右,其原因是升高温度,会提高反应速率,但平衡逆向移动,CO的平衡转化率下降,实际生产中应综合考虑速率和平衡两个方面.
3. 已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
 已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )| A. | 若A为非金属单质,则它与Mg反应的产物,其阴阳离子个数比可能为2:3 | |
| B. | 若A为非金属单质,则其组成元素在周期表中的位置肯定处于第二周期第VA族 | |
| C. | 若D的浓溶液在常温下能使铁、铝发生钝化,则A一定为非金属单质 | |
| D. | 若A是共价化含物,0.l mol的A分子中含有的电子数可能为NA (NA为阿佛加德罗常数的值) |
10.几种短周期元素的原子半径及主要化合价见下表:
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.186 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +1 | -2,+4,+6 | +3 | -2 |
| A. | 离子的还原性:T2->Z2- | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物对应水化物的碱性:Y>R>X | |
| D. | 形成氢化物的沸点:Z>T |
7.下列离子方程式书写正确的是( )
| A. | 石炭酸与NaOH溶液混合:H++OH-→H2O | |
| B. | 稀HNO3洗涤试管中的银镜:Ag+NO3-+2H+═Ag++NO↑+H2O | |
| C. | 乙烯使酸性KMnO4褪色:5C2H4+12MnO4-+36H+→12Mn2++10CO2↑+28H2O | |
| D. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热: |
4.X、Y、Z是短周期的三种相邻元素,X和Y在同一周期,Y和Z在同一主族,这三种元素原子的最外层电子数之和为19,且原子序数之和为41,则X、Y、Z的元素符号分别为( )
| A. | N、O、S | B. | Cl、S、O | C. | Si、P、N | D. | S、Cl、F |
5.下列变化过程中肯定要放出热量的是( )
| A. | H2→H+H | B. | H+Cl→HCl | ||
| C. | H2O(l)→H2O(g) | D. | CaCO3$\stackrel{高温}{→}$CaO+CO2 |