��Ŀ����
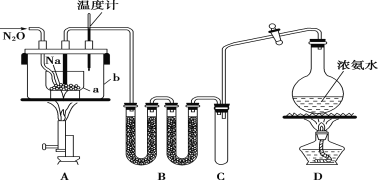
����Ŀ��������һ��ǿ����������⻯��ˮ��Һ������Ӧ���������͵��ʵ⡣��Ӧ�����Һ�е����̪����Һ��Ϊ��ɫ��
��1����д���÷�Ӧ�Ļ�ѧ����ʽ����_____��
��2���÷�Ӧ��ϵ�л������Ż�ѧ��Ӧ����I2(aq) + I-(aq)![]() I3-(aq)����Ӧ���ƽ�ⳣ������ʽΪ��____��
I3-(aq)����Ӧ���ƽ�ⳣ������ʽΪ��____��
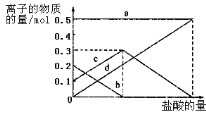
��3��������ͼ�����㷴Ӧ����3-18s����I2��ʾ�ķ�Ӧ����Ϊ_____��

��4��Ϊ̽��Fe2+������O3����I-��Ӧ��Ӱ�죬��O3ͨ�뺬Fe2+��I-�Ļ����Һ�С���Ԥ����Fe2+�Ĵ��ڿ��������Ļ�ѧ��Ӧ�����������������磺�������ӱ���������Ϊ�ⵥ�������� ______���� _____���÷�Ӧ�Ĺ���������������Һ��pH������߷�Ӧ�����Т�-��ת���ʣ�ԭ���ǣ�____ ��
��5������I2�������Կɲⶨ��������ĺ����������ǽ������е���ת��ΪH2SO3��Ȼ���Ե���Ϊָʾ������һ��Ũ�ȵ�I2��Һ���еζ����ۺ�����������Ӧ������֪ʶ������֪������ǿ����ϵ��ȷ����____������ţ���
a. Fe3+�� I2 b. O3�� Fe3+ c. I2�� O2 d. I2��SO42-
���𰸡�O3+2KI+H2O=O2+I2+2KOH K=![]() 5.5��10-4molL-1s-1 �������ӱ���������Ϊ������ ������ˮ������������������ Fe3���γ�Fe(OH)3����������OH����ʹ��ӦIƽ�⳯����Ӧ�����ƶ����ٽ�I��ת�� abd
5.5��10-4molL-1s-1 �������ӱ���������Ϊ������ ������ˮ������������������ Fe3���γ�Fe(OH)3����������OH����ʹ��ӦIƽ�⳯����Ӧ�����ƶ����ٽ�I��ת�� abd
��������
(1)������һ��ǿ����������⻯��ˮ��Һ������Ӧ���������͵��ʵ�,��Ӧ�����ӷ���ʽΪ: O3+2KI+H2O=O2+I2+2KOH ����ˣ�������ȷ����: O3+2KI+H2O=O2+I2+2KOH ��
(2)����ƽ�ⳣ���ĸ����֪����ӦI2(aq) + I-(aq)![]() I3-(aq)��ƽ�ⳣ������ʽΪ:K=
I3-(aq)��ƽ�ⳣ������ʽΪ:K=![]() ����ˣ�������ȷ����: K=
����ˣ�������ȷ����: K=![]() ��
��
(3)��Ӧ����3-18s��I3-��Ũ�ȱ仯Ϊ:11.8![]() 10-3mol/L-3.5
10-3mol/L-3.5![]() 10-3mol/L=8.3
10-3mol/L=8.3![]() 10-3mol/L,��Ӧ����3-18s ����I3-��ʾ�ķ�Ӧ����Ϊ:V(I3-)=8.3
10-3mol/L,��Ӧ����3-18s ����I3-��ʾ�ķ�Ӧ����Ϊ:V(I3-)=8.3![]() 10-3mol/L��15s=5.5
10-3mol/L��15s=5.5![]() 10-3 molL-1s-1����ѧ��Ӧ�����뻯ѧ������������,��V(I3-)=v(I2)= 8.3
10-3 molL-1s-1����ѧ��Ӧ�����뻯ѧ������������,��V(I3-)=v(I2)= 8.3![]() 10-3mol/L��15s=5.5
10-3mol/L��15s=5.5![]() 10-3 molL-1s-1����ˣ�������ȷ����: 5.5
10-3 molL-1s-1����ˣ�������ȷ����: 5.5![]() 10-3 molL-1s-1��
10-3 molL-1s-1��
(4)��Fe2+�Ļ�ԭ�Խ�ǿ,���������ӱ���������Ϊ�����ӣ�
��ˣ�������ȷ����:�������ӱ���������Ϊ�����ӣ�
������������Һ������ˮ�ⷴӦ������������,�ù���������OH-,ʹ��Ӧ��I����ƽ����������Ӧ�����ƶ�,�ٽ�I-ת��,����˷�Ӧ(��)��I-��ת���ʣ�
��ˣ��������:������ˮ������������������; Fe3+�γ�Fe(OH)3����������OH-��ʹ��Ӧ��I����ƽ����������Ӧ�����ƶ�,�ٽ�I-ת����
(5)����I2�������Կɲⶨ��������ĺ�����������ӦΪH2SO3+I2+H2O=4H++SO42-+2I-��֤��������I2> SO42-��������Ϸ�������֪֪ʶ������֪��������: Fe3��> I2��O3> Fe3��,
��ˣ�������ȷ����:abd��