题目内容
在一支量程为20mL的酸式滴定管中盛放盐酸,液面恰好在a mL刻度处,把管内液体全部放出,所得液体体积是( )
| A、a mL |
| B、(20-a)mL |
| C、大于(20-a)mL |
| D、大于a mL |
考点:计量仪器及使用方法
专题:化学实验常用仪器
分析:滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,据此即可解答.
解答:
解:滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,20mL滴定管中实际盛放液体的体积大于20mL,因此,一支20mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,还有满刻度以下的溶液一并放出,总量超过(20-a)mL,盛入量筒内,所得液体体积一定是大于(20-a)mL,
故选C.
故选C.
点评:本题考查了酸式滴定管的结构,注意滴定管的“0”刻度在上端,满刻度在下端,滴定管满刻度以下还有一段空间没有刻度,是解答的关键,题目难度不大.

练习册系列答案
相关题目
韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”.则关于“暖冰”的判断正确的是( )
| A、“暖冰”中存在离子键 |
| B、“暖冰”中水分子的O-H键是非极性键 |
| C、“暖冰”的密度大,有导电性和导热性 |
| D、水凝固形成20℃时的“暖冰”所发生的变化是物理变化 |
下列离子方程式书写正确的是( )
| A、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | ||||
B、用铜作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| C、将H2O2滴加到酸性KMnO4溶液中:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O | ||||
| D、向含有FeBr2溶液中通入少量的Cl2:2Fe2++Cl2=2Fe3++2Cl- |
微粒甲与微粒乙在溶液中的转化关系如图所示: ,微粒甲不可能是( )
,微粒甲不可能是( )
 ,微粒甲不可能是( )
,微粒甲不可能是( )| A、CO2 |
| B、NH4+ |
| C、Al3+ |
| D、SiO2 |
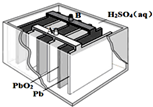 铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:
铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
| A、放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l) |
| B、铅蓄电池广泛用于汽车启动电源,可以边使用边充电,充电时,应将充电电源的正极与铅蓄电池的接线柱A相接 |
| C、实验室用铅蓄电池做电源精炼粗铜时,应将粗铜与接线柱B相连接 |
| D、铅蓄电池做电源电解AgNO3溶液,当有标况下11.2升O2产生时,消耗2mol H2SO4 |
下列有关说法错误的是( )
| A、医药中常用酒精消毒,是因为酒精能使细菌蛋白变性 |
| B、聚酯纤维、光导纤维都属于有机高分子材料 |
| C、对废旧电池回收处理是为了防止重金属污染水源和土壤 |
| D、绿色化学的核心是从源头上减少和消除化工生产对环境的污染 |
科学家及一些实业家的贡献对科学的发展起着积极地推动作用.下列对有关科学家及其发明创造的叙述,错误的是( )
| A、拉瓦锡证明了化学反应中的质量守恒,建立了燃烧的新理论 |
| B、舍勒发现了氯气,凯库勒提出了苯的结构式 |
| C、侯德榜发明了“候氏制碱”法,吴蕴初开创了中国的氯碱工业 |
| D、道尔顿、汤姆孙、卢瑟福和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
将如图所示实验装置的K闭合,下列判断错误的是( )
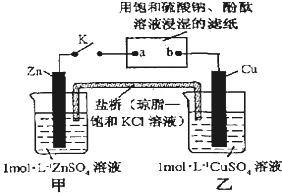

| A、盐桥中的K+移向乙池 |
| B、电子沿Zn→a→b→Cu路径流动 |
| C、b电极上的反应式为4OH-4e-=O2↑+2H2O |
| D、片刻后可观察到滤纸a点变红色 |