题目内容
铋(Bi)是第VA族元素,+5价Bi的化合物氧化性大于MnO4—。某反应中反应物与生成物有:NaMnO4、NaBiO3、Na2SO4、MnSO4、Bi2(SO4)3、H2O和一种未知物X。下列关于该反应的描述中不正确的是( )
| A.X是H2SO4 |
| B.反应中Mn原子与Bi原子个数比为5:2 |
| C.该反应中NaBiO3作氧化剂 |
| D.该反应中Na2SO4既不是氧化产物,又不是还原产物 |
B
解析试题分析: +5价Bi的化合物氧化性大于MnO4-,则发生NaBiO3+X+MnSO4→NaMnO4+Na2SO4+Bi2(SO4)3+H2O,A.由原子守恒可知,X为H2SO4,故A正确;B.由电子守恒可知,反应中Mn原子与Bi原子个数比为2:5,故B错误;C.Bi元素的化合价降低,则该反应中NaBiO3作氧化剂,故C正确;D.该反应中只有Bi、Mn元素的化合价变化,则该反应中Na2SO4既不是氧化产物,又不是还原产物,故D正确;所以答案选B
考点:考查氧化还原反应的相关知识点

试管内壁的硫磺可以用热的KOH溶液来洗涤:3S+6KOH==K2SO3+2K2S+3H2O,该反应中,被氧化与被还原的硫原子个数比为
| A.1:2 | B.2:1 | C.1:1 | D.3:2 |
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性溶液中可以发生反应产生Cl2,下列关于混盐CaOCl2的有关判断不正确的是(NA为阿伏加德罗常数)
| A.该混盐在酸性溶液中产生1mol Cl2时转移的电子数为NA |
| B.该混盐的水溶液具有漂白性 |
| C.该混盐中氯元素的化合价为+1和-1价 |
| D.该混盐具有较强的还原性 |
下列过程中没有发生氧化还原反应的是
| A.天然气燃烧提供热量 |
| B.氯水使红色纸张褪色 |
| C.钢铁制品在空气中被腐蚀 |
| D.二氧化硫通人品红溶液中,溶液褪色 |
从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O = 7Cu2S+5FeSO4+12H2SO4下列说法正确的是
| A.Cu2S既是氧化产物,又是还原产物 |
| B.产物中的SO42-有一部分是氧化产物 |
| C.5molFeS2发生反应时,有l0mol电子转移 |
| D.FeS2只做还原剂 |
利用常温下氨跟氯气能发生置换反应的性质,氯碱工业生产中用来检查氯气是否泄漏,其模拟装置如图。下列有关说法错误的是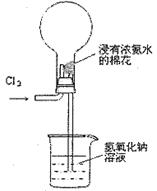
| A.烧瓶中会出现白烟 |
| B.烧瓶中会立即出现喷泉 |
| C.烧瓶中发生的反应表明常温下氨气有还原性 |
| D.烧瓶中还发生化合反应 |
已知反应:Na2O2 + SO2 = Na2SO4,则下列判断正确的是
| A.硫元素被还原 |
| B.二氧化硫是还原剂 |
| C.过氧化钠既是氧化剂又是还原剂 |
| D.二氧化硫既不是氧化剂也不是还原剂 |
火法炼铜首先要焙烧黄铜矿,反应为:CuFeS2+O2 Cu2S+FeS+SO2 则下列说法正确的是
Cu2S+FeS+SO2 则下列说法正确的是
| A.CuFeS2既是氧化剂又是还原剂,硫元素既被氧化又被还原 | B.每生成1molSO2转移6mol电子 |
| C.SO2既是氧化产物又是还原产物,FeS只是还原产物 | D.每转移1.2 mol电子,有0.3 mol氧气被还原 |

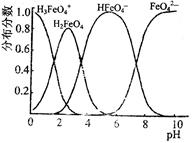
 4Fe(OH)3↓+8OH—+3O2↑,则K2FeO4可以在水处理中的作用是 。
4Fe(OH)3↓+8OH—+3O2↑,则K2FeO4可以在水处理中的作用是 。