题目内容
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是 ( )
加入的物质 | 结论 | |
A | 50mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.05molCaO | 溶液中 |
A. A B. B C. C D. D
【答案】D
【解析】A、H2SO4提供H+的物质的量为50×10-3×2×1mol=0.1mol,是CO32-物质的量的2倍,因此反应方程式为Na2CO3+H2SO4=Na2SO4+CO2↑+H2O,从而得出c(Na+)=2c(SO42-),故A错误;B、发生的离子反应是CO32-+2H+=CO2↑+H2O,溶液的pH降低,c(Na+)增大,故B错误;C、CO32-发生:CO32-+H2O ![]() HCO3-+OH-,加水稀释,离子浓度降低,平衡向正反应方向进行,促进水的电离,水电离出的c(H+)×c(OH-)增大,故C错误;D、发生CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,c(OH-)增大,c(HCO3-)浓度降低,因此此比值增大,故D正确。
HCO3-+OH-,加水稀释,离子浓度降低,平衡向正反应方向进行,促进水的电离,水电离出的c(H+)×c(OH-)增大,故C错误;D、发生CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,c(OH-)增大,c(HCO3-)浓度降低,因此此比值增大,故D正确。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案【题目】
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1—36号元素),与中学常见的长式元素周期表相比,第一到第十八可看成族,k为Fe元素。试根据扇形周期表已填入元素回答问题:
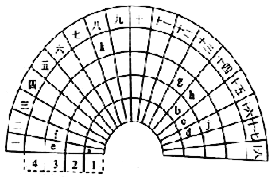
(1)c的基态原子中,核外存在______对自旋相反的电子。元素x与g同族且比g多三个电子层,元素x的价电子排布式为____________。
(2)e、f、g的第一电离能由大到小的顺序为________(用元素符号表示)。
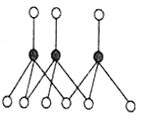
(3)d与j所形成的某种化合物固态时通常以三聚体的环状形式存在,如下图所示,其中j的原子杂化方式为_________。
(4)b和d所形成的一种三原子分子与c和d形成的一种化合物互为等电子体,则满足上述条件的c和d形成的化合物的化学式是__________________。
(5)b和h的有关化学键键能如下表所示,简要分析和解释下列有关事实:
化学键 | b-b | b-a | b-b | h-a |
键能/kj·mol-1 | 356 | 413 | 226 | 318 |
b与a形成化合物的种类远大于h与a形成化合物的种类,从能量的角度分析原因_____________。
(6)下图为e与x所形成的合金立方晶系晶胞图,晶胞棱长为748.8pm。

①若把一类金属原子全部抽掉,剩余的金属原子与扇形周期表中哪种已填入元素形成的单质晶型相同,该单质名称为___________。
②原子坐标参数,表示晶胞内部各原子的相对位置。其中坐标参数A处x为(0,0,0);B处e为(0,0, ![]() );C处x坐标为(
);C处x坐标为(![]() ,
, ![]() ,0)。则D处x的坐标参数为___________。
,0)。则D处x的坐标参数为___________。
③该晶体的密度计算式为___________g/cm3(已知x的相对原子质量为204)