题目内容
15.下列有关物质用途的说法错误的是( )| A. | 可用铝槽密闭盛装浓硫酸 | |
| B. | 工业上利用蛋白质的水解反应生产肥皂和甘油 | |
| C. | 乙醇可用作汽车燃料 | |
| D. | 食醋可用于消除暖水瓶中的水垢 |
分析 A.常温下铝于浓硫酸发生钝化反应;
B.油脂可发生皂化反应;
C.乙醇为清洁燃料;
D.醋酸酸性比碳酸强.
解答 解:A.常温下铝于浓硫酸发生钝化反应,在表面生成一层致密的氧化物膜而阻碍反应的进行,可用铝槽密闭盛装浓硫酸,故A正确;
B.蛋白质水解生成氨基酸,二油脂可发生皂化反应生成肥皂,故B错误;
C.乙醇燃烧放出大量的热,生成二氧化碳和水,为清洁燃料,故C正确;
D.醋酸酸性比碳酸强,则可用食醋消除暖水瓶中的水垢,故D正确.
故选B.
点评 本题综合考查元素化合物知识,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
12.已知:
①CaO(s)+H2O(1)═Ca(OH)2(aq);△H1
②CaO(s)+2HCl(g)═CaCl2(s)+H2O(1);△H2
③NH3(g)+HCl(g)═NH4Cl(s);△H3
④Ca(OH)2(aq)+2NH4Cl(s)═CaCl2(aq)+2NH3(g)+2H2O(1);△H4>0
下列关于上述反应焓变的判断正确的是( )
①CaO(s)+H2O(1)═Ca(OH)2(aq);△H1
②CaO(s)+2HCl(g)═CaCl2(s)+H2O(1);△H2
③NH3(g)+HCl(g)═NH4Cl(s);△H3
④Ca(OH)2(aq)+2NH4Cl(s)═CaCl2(aq)+2NH3(g)+2H2O(1);△H4>0
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0 | B. | △H4=△H1-△H2-2△H3 | ||
| C. | △H4=△H2-△H1-2△H3 | D. | △H4-△H1-△H2<0 |
6.下列关于热化学反应的描述中正确的是( )
| A. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9 kJ•mol-1,则CH3OH的燃烧热为192.9 kJ•mol-1 | |
| C. | H2(g)的燃烧热是285.8 kJ•mol-1,则2H2O(g)═2H2(g)+O2(g);△H=+571.6 kJ•mol-1 | |
| D. | 葡萄糖的燃烧热是2800 kJ•mol-1,则1/2 C6H12O6 (s)+3O2 (g)═3CO2 (g)+3H2O ( l );△H=-1400 kJ•mol-1 |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,1mol水的体积约为22.4L | |
| B. | 3.4gOH-中含有的电子的数目为0.2NA | |
| C. | 标准状况下,11.2 LCO2和SO2混合气体中含NA个氧原子 | |
| D. | 1mol氖气和1mol氧气体积相同 |
20.相同状况下,下列气体占有的体积最大的是( )
| A. | 64g SO2 | B. | 16g O2 | C. | 34g H2S | D. | 3g H2 |
7.下面列出的BaSO4在医学上用做钡餐的理由,其中正确的是( )
①既不溶于水又不溶于酸 ②对人体有较大毒性 ③不易被X射线透过 ④有治疗疾病的作用.
①既不溶于水又不溶于酸 ②对人体有较大毒性 ③不易被X射线透过 ④有治疗疾病的作用.
| A. | 只有① | B. | ①和③ | C. | ①和④ | D. | ②和③ |
4.一块已被部分氧化为Na2O的钠块10.8g,将其投入一定量水中,最终得到1L 0.4mol•L-1的NaOH溶液,则原固体中氧化钠的质量是( )
| A. | 8.5g | B. | 10.8g | C. | 6.2g | D. | 4.6g |
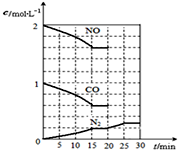 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.