题目内容
【题目】
(1)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O(用“双线桥法”表示电子转移的方向和数目),该反应中氧化剂是_____________,氧化产物与还原产物的物质的量之比为_____________。
(2)______molH2O中共含有9.03×1022个原子,其质量为_______。
(3)配平下列氧化还原反应方程式:
___KMnO4+___H2S+__H2SO4(稀)===__MnSO4+__S↓+__K2SO4+__H2O
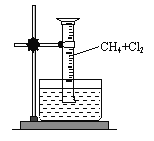
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol则被氧化的NH3在标准状况下的体积为______L。
【答案】
(1)![]() HNO33:2(2)0.050.9g
HNO33:2(2)0.050.9g
(3)2KMnO4+5H2S+3H2SO4(稀)=2MnSO4+5S↓+1K2SO4+8H2O
(4)22.4
【解析】
试题分析:(1)该氧化还原反应中的,化合价升高的是铜元素,化合价降低的是硝酸中的氮元素,转移电子数为6mol,双线桥法表示电子转移的方向和数目如下所示: ,化合价升高的是铜元素,被氧化,化合价降低的元素是氮元素,所在的反应物硝酸是氧化剂,金属铜是还原剂,氧化产物是Cu(NO3)2,还原产物是NO,氧化产物与还原产物的物质的量之比为3:2;
,化合价升高的是铜元素,被氧化,化合价降低的元素是氮元素,所在的反应物硝酸是氧化剂,金属铜是还原剂,氧化产物是Cu(NO3)2,还原产物是NO,氧化产物与还原产物的物质的量之比为3:2;
(2)9.03×1022个原子的物质的量为![]() =0.15mol,1个水分子含有3个原子,故水的物质的量为0.15mol÷3=0.05mol,故水的质量为0.05mol×18g/mol=0.9g;
=0.15mol,1个水分子含有3个原子,故水的物质的量为0.15mol÷3=0.05mol,故水的质量为0.05mol×18g/mol=0.9g;
(3)反应中KMnO4→MnSO4,Mn元素化合价由+7降低为+2,共降低5价,H2S→S,S元素化合价由-2价升高为0价,共升高为2价,化合价升降最小公倍数为10,故KMnO4的系数为2,H2S的系数为5,再根据原子守恒配平其它物质的系数,配平后方程式为:2KMnO4+5H2S+3H2SO4(稀)=2MnSO4+5S↓+1K2SO4+8H2O;
(4)被氧化的氨气生成氮气,根据方程式可知生成氨气的物质的量为1.5mol×1/3=0.5mol,根据氮原子守恒可知被氧化的氨气的物质的量为0.5mol×2=1mol,故被氧化氨气的体积为1mol×22.4L/mol=22.4L。

【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施