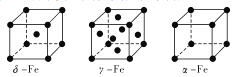
题目内容
【题目】【选修5——有机化学基础】
某新型有机化学材料G的合成路线如图所示,请回答下列问题:
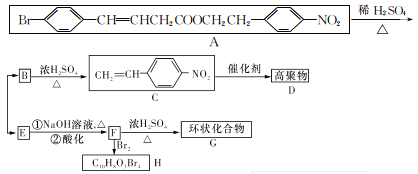
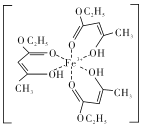
(1)F分子中的含氧官能团名称为_______。
(2)高聚物D的结构简式是_______。
(3)写出反应A→B+E的化学方程式:________。
(4)F→H的反应类型有______、_________。
(5)B的同分异构体有多种,其中官能团种类不变,能与FeCl3溶液发生显色反应,核磁共振氢谱显示有6组峰,且峰面积之比为1:1:1: l:2:3的同分异构体有_____种。
(6)参照上述合成路线,以CH3CHBrCOOCH3为原料(无机试剂任选),设计制备聚乳酸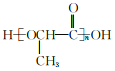 的合成路线_____________________。
的合成路线_____________________。
【答案】 羟基、羧基 
![]() +H2O
+H2O![]()
![]() +
+![]() 加成反应 取代反应 (顺序可互换) 20
加成反应 取代反应 (顺序可互换) 20 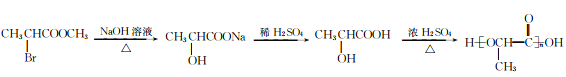
【解析】本题主要考查有机物的结构与性质。
(1)A→B+E发生酯的水解反应,E含有羧基和溴原子,E→F发生溴原子与羟基的取代反应,因此,F分子中的含氧官能团名称为羟基、羧基。
(2)高聚物D是C的加聚产物,D的结构简式是 。
。
(3)反应A→B+E发生酯的水解反应,反应的化学方程式:![]() +H2O
+H2O![]()
![]() +
+![]() 。
。
(4)F→H发生碳碳双键与溴的加成反应和酚与溴的取代反应,反应类型有加成反应、取代反应。
(5)B为![]() ,B的同分异构体能与FeCl3溶液发生显色反应,表明该物质含有酚羟基,核磁共振氢谱显示有6组峰,且峰面积之比为1:1:1:1:1:2:3,表明该物质含有6种氢原子,且6种氢原子数目之比为1:1:1:1:2:3。符合上述条件的该物质的分子结构中,苯环侧链为—CH2CH3、—OH、—NO2的有10种,苯环侧链为—CH2NO2、—CH3、—OH的有10种,共20种。
,B的同分异构体能与FeCl3溶液发生显色反应,表明该物质含有酚羟基,核磁共振氢谱显示有6组峰,且峰面积之比为1:1:1:1:1:2:3,表明该物质含有6种氢原子,且6种氢原子数目之比为1:1:1:1:2:3。符合上述条件的该物质的分子结构中,苯环侧链为—CH2CH3、—OH、—NO2的有10种,苯环侧链为—CH2NO2、—CH3、—OH的有10种,共20种。
(6)以CH3CHBrCOOCH3为原料(无机试剂任选),制备聚乳酸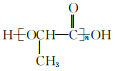 的合成思路:将CH3CHBrCOOCH3水解为CH3CHBrCOOH,再水解为CH3CHOHCOOH,最后缩聚为聚乳酸。合成路线:
的合成思路:将CH3CHBrCOOCH3水解为CH3CHBrCOOH,再水解为CH3CHOHCOOH,最后缩聚为聚乳酸。合成路线: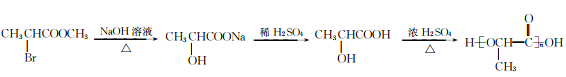 。
。

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】下列有关物质的实验操作、现象及结论描述正确的是( )
选项 | 实验操作及现象 | 结论 |
A | 用铂丝蘸取某待测液在酒精灯外焰上灼烧,火焰呈紫色(透过蓝色钴玻璃) | 待测试液中一定含有钾元素,可能含钠元素 |
B | 向某无色溶液中通入过量的CO2气体,有白色沉淀产生 | 该溶液中一定含有SiO32– |
C | 向品红溶液中通入某气体后,溶液褪色 | 该气体一定是SO2 |
D | 向NaOH溶液中滴加MgCl2溶液,产生白色沉淀,继续滴加FeCl3溶液产生红褐色沉淀 | Fe(OH)3的溶解度小于Mg(OH)2的溶解度 |
A. A B. B C. C D. D
【题目】四氯化钛(TiCl4)是生产金属钛及其化合物的重要中间体。室温下,四氯化钛为无色液体。某化学兴趣小组同学以TiO2和CCl4为原料在实验室制取液态TiCl4,装置如下图所示:

有关信息如下:
①反应原理:TiO2(s)+CCl4(g) ![]() TiCl4(g)+CO2(g)。
TiCl4(g)+CO2(g)。
②反应条件:无水无氧且加热。
③有关物质性质如下表所示:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | -23 | 76 | 与TiCl4互溶 |
TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题:
(1)装置F中有氮气生成,该反应的化学方程式为_______________________。
(2)实验装置依次连接的顺序为F→B→______。
(3)实验开始前首先点燃____处(填“D”或“F”)酒精灯,目的是______________。
(4)E装置不能换成B装置,理由是______________。
(5)欲分离装置C中的液态混合物,所采用操作方法的名称是______________。
(6)TiCl4是制取航天航空工业材料钛合金的重要原料。某钛合金含有的元素还有Al和Si等。已知在常温下,钛是一种耐强酸、强碱的金属,请设计实验检验其中的Si元素________________。