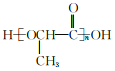题目内容
【题目】已知 X、Y、Z、W 四种元素分别是元素周期表中连续 3 个短周期的元素,且原子序数 依次增大.X、W 同主族,Y、Z 为同周期的相邻元素.W 原子的质子数等于 Y、Z 原子最 外层电子数之和.Y 与 X 形成的分子中有 3 个共价键.Z 原子最外层电子数是次外层电子 数的 3 倍.试推断:
(1)Z 离子的结构示意图 .
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的电子式 为;含有离子键和共价键的化合物的化学式为 .
(3)由 X、Y、Z 所形成的常见离子化合物是 (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为 .
(4)用电子式表示W与Z形成W2Z化合物的形成过程: .
【答案】
(1)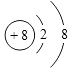
(2)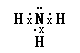 ;Na2O2
;Na2O2
(3)NH4NO3;NH4++OH﹣ ![]() NH3↑+H2O
NH3↑+H2O
(4)![]()
【解析】解:Z原子最外层电子数是次外层电子数的3倍,Z原子只能有2个电子层,最外层电子数为6,则Z为O元素;Y与X形成的分子中有3个共价键,四种元素分别是元素周期表中连续 3 个短周期的元素,Y的原子序数小于O元素,则Y为N元素、X为H元素;W原子的质子数等于Y、Z原子最外层电子数之和,W原子质子数=5+6=11,则W为Na元素,(1)Z为O元素,氧离子的核电荷数为8、核外电子总数为10,其离子结构示意图为: 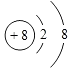 ,所以答案是:
,所以答案是: 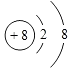 :(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物是氨气,氨气的电子式为
:(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物是氨气,氨气的电子式为  ; 含有离子键和非极性共价键的化合物为过氧化钠,过氧化钠的化学式为:Na2O2 ,
; 含有离子键和非极性共价键的化合物为过氧化钠,过氧化钠的化学式为:Na2O2 ,
所以答案是:  ;Na2O2;(3)由X、Y、Z所形成的常见离子化合物是NH4NO3 , W的最高氧化物的水化物为NaOH,二者反应的离子方程式为:NH4++OH﹣
;Na2O2;(3)由X、Y、Z所形成的常见离子化合物是NH4NO3 , W的最高氧化物的水化物为NaOH,二者反应的离子方程式为:NH4++OH﹣ ![]() NH3↑+H2O,
NH3↑+H2O,
所以答案是:NH4NO3;NH4++OH﹣ ![]() NH3↑+H2O;(4)W2Z为Na2O,氧化钠属于离子化合物,用电子式表示氧化钠的形成过程为
NH3↑+H2O;(4)W2Z为Na2O,氧化钠属于离子化合物,用电子式表示氧化钠的形成过程为 ![]() ,
,
所以答案是: ![]() .
.

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣5molL﹣1 | K1=4.4×10﹣7molL﹣1 K2=5.6×10﹣11molL﹣1 | 3.0×10﹣8 molL﹣1 |
请回答下列问题:
(1)同浓度的CH3COO﹣、HCO3﹣、CO32﹣、ClO﹣结合H+的能力由强到弱的顺序为_____。
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母序号,下同).
A.c(H+) B.![]() C.c(H+)c(OH﹣)
C.c(H+)c(OH﹣)
D.![]() E.
E. 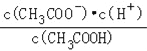
若升高该溶液温度(不考虑醋酸挥发),上述5种表达式的数据增大的是_____.
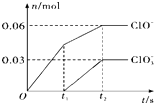
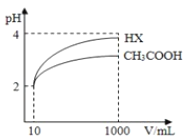
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数_____(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)醋酸的溶液中水电离出来的c(H+),理由是_____.
(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液PH=7,该溶液显_____(填“酸”、“碱”或“中”)性.将此温度下PH=1的H2SO4溶液aL与PH=11的NaOH溶液bL混合,若所得混合液PH=2,则a:b=_____。