题目内容
2.在一定条件下,反应N2+3H2?2NH3在10L恒容密闭容器中进行,测得2min内氮气的物质的量由20mol减少到8mol,则2min内氮气的化学反应速率为( )| A. | 1.2mol•L-1•min-1 | B. | 0.8mol•L-1•min-1 | ||
| C. | 1.0mol•L-1•min-1 | D. | 0.6mol•L-1•min-1 |
分析 2min内氮气的物质的量由20mol减少到8mol,△C=20mol-8mol=12mol,根据v=$\frac{△c}{△t}$计算2min内N2的化学反应速率.
解答 解:2min内,N2的物质的量由20mol减少到8mol,则v(N2)=$\frac{△c}{△t}$=$\frac{20mol-8mol}{\frac{10L}{2min}}$=0.6 mol•L-1•min-1,
故选D.
点评 本题考查化学反应速率的计算,明确计算公式即可解答,注意利用浓度的变化量计算,题目难度不大.

练习册系列答案
相关题目
7.中共中央、国务院于2015年5月5日发布了《关于加快生态文明建设的意见》,5月6日北京市公布禁止露天烧烤地点,取缔各类露天烧烤.下列说法正确的是( )
| A. | 在烧烤过程中,肉类中的蛋白质在高温下发生变性 | |
| B. | 有部分烧烤摊使用了地沟油,地沟油经过精炼后可以食用 | |
| C. | 为了食品卫生,鼓励烧烤摊大量使用一次性竹签 | |
| D. | 露天烧烤产生的大量PM2.5能在空气中形成胶体 |
17.下列关于有机物的说法中正确的是( )
| A. | 甲烷、一氯甲烷、二氯甲烷等均属于烷烃 | |
| B. | 乙醇不与任何酸反应 | |
| C. | 乙酸不能与金属Na反应 | |
| D. | 乙酸乙酯能发生水解反应 |
7.下列有关糖类、油脂、蛋白质的说法中,不正确的是( )
| A. | 淀粉和纤维素都是高分子化合物 | |
| B. | 葡萄糖、油脂和蛋白质都能发生水解反应 | |
| C. | 糖类、油脂、蛋白质均含有C、H、O元素 | |
| D. | 植物油和动物脂肪的主要成分都是高级脂肪酸甘油酯 |
14.下列说法中正确的是( )
| A. | 乙醛与新制Cu(OH)2悬浊液反应生成红色的Cu2O沉淀 | |
| B. | 银镜反应中醛发生的是还原反应 | |
| C. | 甲醛、乙醛、丙醛都没有同分异构体 | |
| D. | 醛类催化加氢后都能得到饱和一元醇 |
11.分子式为C9H12O的有机物,有一个苯环、一个烃基,则它属于酚类的结构可能有( )
| A. | 2种 | B. | 4种 | C. | 5种 | D. | 6种 |
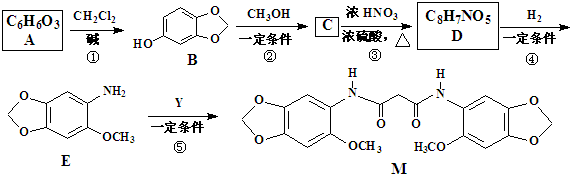

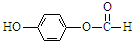 和
和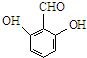 、
、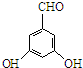 (其中两种)
(其中两种) .
.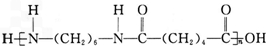 +(2n-1)H2O.
+(2n-1)H2O.