题目内容
【题目】从制造印刷电路板的腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液,处理流程如图:
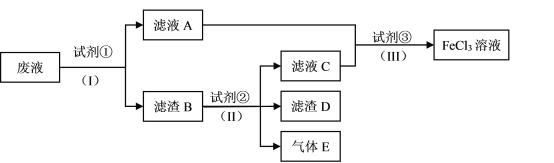
请回答下列问题:
(1)试剂①为___、试剂③为___。
(2)滤渣B中主要含有___。
(3)步骤(Ⅱ)的化学方程式为___。
(4)某Fe2(SO4)3溶液可能含有Fe2+,从下列试剂中选择检验Fe2+存在的最佳试剂___(填字母)。若存在Fe2+,则上述检验的实验现象为___。
A.氢氧化钠溶液 B.酸性KMnO4溶液 C.氯水 D.KSCN溶液
【答案】Fe Cl2 Fe、Cu Fe+2HCl=FeCl2+H2↑ B 酸性KMnO4溶液紫(红)色褪去
【解析】
题中通过制造印刷电路板的腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液,因此可推断得出滤渣D是Cu,试剂①为铁,生成的的滤液A是FeCl2,滤渣B中含有过量的铁和生成的铜,加入的试剂②要除去铁,试剂②应是稀盐酸,生成的滤液C也是FeCl2,气体E是氢气。
(1)由以上分析可知,试剂①为铁粉或Fe;要将FeCl2氧化为FeCl3,且不引入新的杂质,试剂③应为氯气或Cl2。答案为:Fe;Cl2;
(2)为了将CuCl2全部转化为Cu,需加入过量的铁粉,因此滤渣B中主要含有Fe、Cu。答案为:Fe、Cu;
(3)步骤(Ⅱ)为往Fe、Cu混合物中加入盐酸,Fe将与盐酸反应,化学方程式为Fe + 2HCl === FeCl2 + H2↑。答案为:Fe+2HCl=FeCl2+H2↑;
(4)某Fe2(SO4)3溶液可能含有Fe2+,选择试剂检验Fe2+存在时,需注意排除Fe3+的干扰,所以最佳试剂是酸性KMnO4溶液,应选B。若存在Fe2+,酸性高锰酸钾会氧化Fe2+生成Fe3+而褪色,则上述检验的实验现象为酸性KMnO4溶液紫(红)色褪去。答案为:B;酸性KMnO4溶液紫(红)色褪去。

 阅读快车系列答案
阅读快车系列答案【题目】实验室利用废铜合金(含少量铁和铝)来制取硫酸铜晶体(CuSO4·5H2O),方案如下:

金属离子生成氢氧化物沉淀的pH可参考下列数据:
Fe3+ | Fe2+ | Cu2+ | Al3+ | |
开始沉淀时的pH | 2.2 | 7.5 | 5.2 | 3.7 |
完全沉淀时的pH | 3.2 | 9.0 | 6.7 | 4.7 |
请回答:
(1)若溶解合金时加入的混酸由2 L 3 mol·L-1硫酸和1 L 2 mol·L-1硝酸混合而成,则反应后生成标准状况下的NO的体积最多为____________L。
(2)加入H2O2的目的是____________。
(3)为保证产品的纯度,M物质最好选用________(填字母),调节pH的范围为____________。
a.Cu(OH)2 b.H2SO4 c.NH3·H2O d.Na2CO3
(4)滤液D中加入硫酸的目的为_______________________________________。
(5)从溶液E制得CuSO4·5H2O晶体所需要的步骤为________、结晶、过滤和干燥。
(6)0.80g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。试确定200℃时固体物质的化学式______________。