题目内容
14.反应C(s)+H2O(g)?CO(g)+H2(g)△H>0.在容积可变的密闭容器中进行,下列条件对其反应速率几乎无影响的是( )| A. | 升高温度 | B. | 增加C的量 | ||
| C. | 将容器的体积缩小一半 | D. | 保持压强不变,充入N2 |
分析 对应反应C(s)+H2O(g) CO(g)+H2(g),有气体参加和生成,则温度、压强都能对化学反应速率产生影响,以此来解答.
CO(g)+H2(g),有气体参加和生成,则温度、压强都能对化学反应速率产生影响,以此来解答.
解答 解:A、升高温度,则反应速率加快,故A不选;
B、碳为纯固体,改变其用量,对化学反应速率无影响,故B选;
C、将容器的体积缩小一半,相当于压强增大,则反应速率加快,故C不选;
D、压强不变充入N2使容器体积增大,则相当于反应体系的压强减小,反应速率减小,故D不选;
故选B.
点评 本题考查影响化学反应速率的因素,注意该反应中有气体参加和生成时解答本题的关键,并学会利用压强及思维转化的方法来分析解答.

练习册系列答案
相关题目
2.下列变化中,不需要破坏化学键的是( )
| A. | NO与O2反应 | B. | 碘加热升华 | C. | 氯酸钾加热分解 | D. | 氯化钠溶于水 |
9.下列物质所用的高分子材料,你认为具有热固性的是( )
| A. | 塑料凉鞋 | B. | 自行车内胎 | ||
| C. | 电线外面的塑料护套 | D. | 电熨斗的塑料部件 |
19.下列反应的离子方程式正确的是( )
| A. | 钠与水:Na+H2O=Na++OH-+H2↑ | |
| B. | 铜与浓硫酸:Cu+2H+=Cu2++H2↑ | |
| C. | 氯气与氢氧化钠溶液:Cl2+OH-=Cl-+H2O | |
| D. | 二氧化硅与氢氧化钠溶液:SiO2+2OH-=SiO32-+H2O |
20.下列物质性质变化的比较,不正确的是( )
| A. | 酸性强弱:HIO4>HBrO4 | B. | 原子半径大小 Na>S>O | ||
| C. | 碱性强弱KOH>NaOH | D. | 金属性强弱Na>Mg>Al |
1.下列事实不能用勒夏特列原理解释的是( )
| A. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 向氯水中加CaCO3后,溶液漂白性增强 | |
| C. | 将氯化铁溶液加热蒸干最终得不到氯化铁固体 | |
| D. | 增大压强,有利于SO2和O2反应生成SO3 |
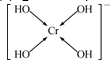 .(若有配位键,用箭号表示)
.(若有配位键,用箭号表示)