题目内容
16.下列说法错误的是( )| A. | 苯环的碳碳键键长都相等 | |
| B. | 苯分子中各个键角都是120° | |
| C. | 一个苯分子中含有三个碳碳单键三个碳碳双键 | |
| D. | 常温下苯是一种不溶于水且密度小于水的液体 |
分析 苯是密度小于水,不溶于水的液体,苯分子中含有的碳碳键是介于双键和单键之间一种特殊的化学键,6个碳碳键完全相同,据此解答.
解答 解:A.苯分子中的6个碳碳键完全相同,故A正确;
B.苯分子中的6个碳碳键完全相同,形成平面正六变形结构,分子中各个键角都是120°,故B正确;
C.苯分子中含有的碳碳键是介于双键和单键之间一种特殊的化学键,故C错误;
D.苯是密度小于水,不溶于水的液体,故D正确;
故选:C.
点评 本题考查了苯的结构及性质,熟悉苯分子的物理性质和结构特点是解题关键,注意苯分子中碳碳键的特殊性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列离子方程式书写正确的是( )
| A. | Ba(OH)2溶液与少量的NaHCO3溶液混合:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O | |
| B. | 次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 金属钾与水反应:K+H2O═K++OH-+H2↑ | |
| D. | 硫酸氢钠与氢氧化钠溶液的反应:H++OH-═H2O |
7.已知酸性  >H2CO3>
>H2CO3>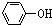 >HCO3-,现要将
>HCO3-,现要将  转变为
转变为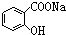 ,可行的方法是( )
,可行的方法是( )
 >H2CO3>
>H2CO3>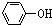 >HCO3-,现要将
>HCO3-,现要将  转变为
转变为 ,可行的方法是( )
,可行的方法是( )| A. | 与足量NaOH溶液共热,再通入足量HCl | |
| B. | 与稀硫酸共热后,加入足量的 NaOH | |
| C. | 与足量NaOH溶液共热,再通入足量的CO2 | |
| D. | 加稀硫酸共热后,再加入足量Na2CO3溶液 |
4.下列各组物质间反应,其中水既不作氧化剂又不作还原剂的氧化还原反应是( )
①F2和H2O ②Na和H2O ③Na2O2和H2O ④P2O5和H2O ⑤Na2O和H2O
⑥Cl2和H2O ⑦NO2和H2O ⑧Al和NaOH溶液.
①F2和H2O ②Na和H2O ③Na2O2和H2O ④P2O5和H2O ⑤Na2O和H2O
⑥Cl2和H2O ⑦NO2和H2O ⑧Al和NaOH溶液.
| A. | ③④⑤⑥⑦ | B. | ①⑤⑦ | C. | ②③⑤⑧ | D. | ③⑥⑦ |
1.某元素X最高价含氧酸的相对分子质量为98,且X的氢化物的分子式不是H2X,则下列说法正确的是( )
| A. | X的最高价含氧酸的分子式可表示为H3XO4 | |
| B. | X是第二周期VA族元素 | |
| C. | X是第三周期ⅥA族元素 | |
| D. | X的最高化合价为+4 |
5.Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒.
(1)电解NaCl溶液生成Cl2的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是HClO
②25℃,Cl2与H2O、NaOH的反应如下:
不直接使用氯水而使用漂白液做消毒剂的原因是K2>K1,反应Ⅱ的有效成分比反应Ⅰ的有效成分大,氯气转化为HClO更充分,次氯酸钠比次氯酸更稳定
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是ClO-+2e-+H2O=Cl-+2OH-
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是>,原因是在相同条件下,次氯酸钠的浓度越大,其分解速率越大
②NaClO分解的化学方程式是2NaClO$\frac{\underline{\;30℃\;}}{\;}$2NaCl+O2↑
③4d~8d,Ⅰ中v(NaClO)=0.047mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
(1)电解NaCl溶液生成Cl2的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是HClO

②25℃,Cl2与H2O、NaOH的反应如下:
| 反应Ⅰ | Cl2+H2O?Cl-+H++HClO K1=4.5×10-4 |
| 反应Ⅱ | Cl2+2OH-?Cl-+ClO-+H2O K2=7.5×1015 |
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是ClO-+2e-+H2O=Cl-+2OH-
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是>,原因是在相同条件下,次氯酸钠的浓度越大,其分解速率越大
②NaClO分解的化学方程式是2NaClO$\frac{\underline{\;30℃\;}}{\;}$2NaCl+O2↑
③4d~8d,Ⅰ中v(NaClO)=0.047mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
