题目内容
资料卡片:溴在水中溶解度不大(稀溴水呈黄色),易溶于CCl4等有机溶剂。
某校化学实验兴趣小组在“探究Cl2、Br2的氧化性”的系列实验中 发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生氧化 还原反应所致,则溶液呈黄色是含 (填化学式)所致。
还原反应所致,则溶液呈黄色是含 (填化学式)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生氧化还原反应所致,则溶液呈黄色是含 (填离子符号)所致。
(3)设计实验并验证:丙同学为验证乙同学的观点,利用下列 提供的试剂,设计出一种
提供的试剂,设计出一种 方案进行了实
方案进行了实 验,并通过观察现象,得出乙同学的观点正确。
验,并通过观察现象,得出乙同学的观点正确。
供选用的试剂:酚酞、CCl4、无水酒精、KSCN溶液、蒸馏水等。
请你写出丙同学选用的试剂是 ,实验中观察到的现象是 。
(4)结论:氧化性:Br2>Fe3+
在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生反应的离子方程式是 。
(5)实验后的思考:根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是 (填离子符号)。
某校化学实验兴趣小组在“探究Cl2、Br2的氧化性”的系列实验中
 发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生氧化
 还原反应所致,则溶液呈黄色是含 (填化学式)所致。
还原反应所致,则溶液呈黄色是含 (填化学式)所致。②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生氧化还原反应所致,则溶液呈黄色是含 (填离子符号)所致。
(3)设计实验并验证:丙同学为验证乙同学的观点,利用下列
 提供的试剂,设计出一种
提供的试剂,设计出一种 方案进行了实
方案进行了实 验,并通过观察现象,得出乙同学的观点正确。
验,并通过观察现象,得出乙同学的观点正确。供选用的试剂:酚酞、CCl4、无水酒精、KSCN溶液、蒸馏水等。
请你写出丙同学选用的试剂是 ,实验中观察到的现象是 。
(4)结论:氧化性:Br2>Fe3+
在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生反应的离子方程式是 。
(5)实验后的思考:根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是 (填离子符号)。
(2)① Br2 ;② Fe3+ (3)KSCN溶液;溶液变红色
(4)2Fe2++Br2=2Fe3++2Br- (5)Fe2+
(4)2Fe2++Br2=2Fe3++2Br- (5)Fe2+
略

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
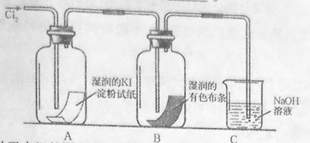

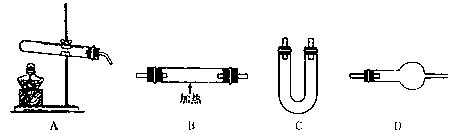
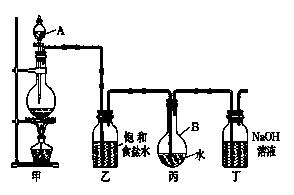
 微粒符号表示 );
微粒符号表示 ); _______________________________________________________________________
_______________________________________________________________________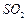 是一种大气污染物,某兴趣小组欲探究
是一种大气污染物,某兴趣小组欲探究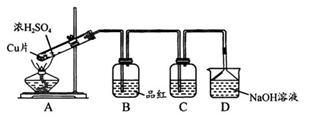
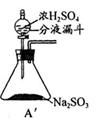


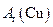 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量 m(H20),由此计算
m(H20),由此计算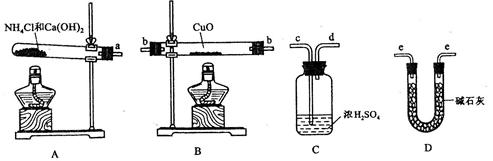
 的是_______________ (填序号);
的是_______________ (填序号); 干燥
干燥 _____和_______________达到实验目的。
_____和_______________达到实验目的。 等离子的卤水为主要原料制备无水
等离子的卤水为主要原料制备无水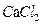 和
和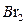 ,流程如下:
,流程如下: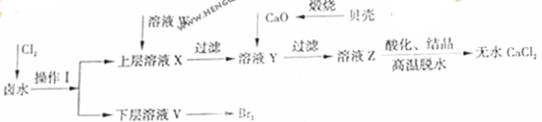
 。
。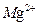 。由表中数据可知,理论上可选择pH最大范围是 。酸化溶液Z时,使用的试剂为 。
。由表中数据可知,理论上可选择pH最大范围是 。酸化溶液Z时,使用的试剂为 。
 气体,下列装置中合理的是 。
气体,下列装置中合理的是 。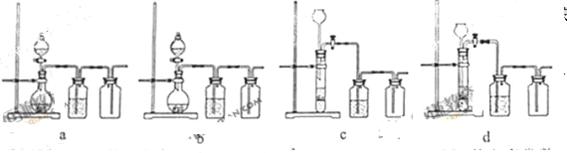
 的电离常数
的电离常数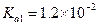 ,
,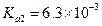 ,
,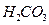 的电
的电 离常数
离常数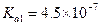 ,
,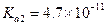 。某同学设计实验验证
。某同学设计实验验证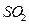 和
和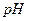 ,若前者的
,若前者的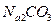 、
、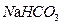 、
、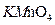 、
、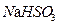 、蒸馏水、饱和石灰水、酸性
、蒸馏水、饱和石灰水、酸性