题目内容
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么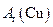 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量 m(H20),由此计算
m(H20),由此计算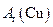 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
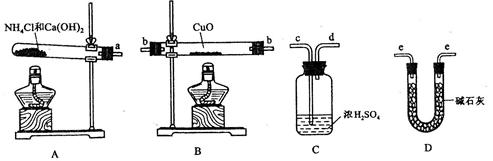
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)=" a" g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大 的是_______________ (填序号);
的是_______________ (填序号);
1Cu0未完全起反应 ② CuO不 干燥
干燥
3Cu0中混有不反应的杂质 ④碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________ _____和_______________达到实验目的。
_____和_______________达到实验目的。
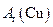 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量 m(H20),由此计算
m(H20),由此计算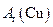 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)=" a" g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大
 的是_______________ (填序号);
的是_______________ (填序号);1Cu0未完全起反应 ② CuO不
 干燥
干燥3Cu0中混有不反应的杂质 ④碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________
 _____和_______________达到实验目的。
_____和_______________达到实验目的。(1)2NH3 + 3CuO
 3Cu + 3H2O + N2↑
3Cu + 3H2O + N2↑(2)a→ e→ b→ e
(3)18a/b — 16
(4)①③
(5)m(CuO)和m(Cu),m(Cu)和m(H2O)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。 提供的试剂,设计出一种
提供的试剂,设计出一种 方案进行了实
方案进行了实 验,并通过观察现象,得出乙同学的观点正确。
验,并通过观察现象,得出乙同学的观点正确。
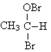
 N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。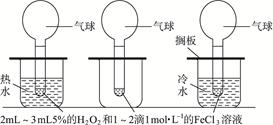
 假设2:既不存在SO32-也不存在ClO-
假设2:既不存在SO32-也不存在ClO- ______
______ L-1H2SO4、1moL
L-1H2SO4、1moL
 测定实验中,加热后的硫酸铜应在空气中冷却后
测定实验中,加热后的硫酸铜应在空气中冷却后 再称量
再称量 思。经过用另一溶液简单处理后,表弟看到了一封有颜色的信,并很快写了回信。小张和表弟所用的溶液分别可能是( )。
思。经过用另一溶液简单处理后,表弟看到了一封有颜色的信,并很快写了回信。小张和表弟所用的溶液分别可能是( )。 