题目内容
3.100mL浓度为2mol•L-1的硫酸跟足量的锌片反应,为增大反应速率,又不影响生产氢气的总量,可采取的方法是( )| A. | 加入适量的5mol•L-1的硫酸 | B. | 加入少量醋酸钠固体 | ||
| C. | 加热 | D. | 加入少量金属钠 |
分析 能增大反应速率且不影响氢气的生产总量,可以通过适当增大氢离子浓度、升高温度、增大反应物接触面积等方法来实现,但不能加入和稀硫酸反应的物质或能生成氢气的物质,据此分析解答.
解答 解:A.适当增大稀硫酸浓度,能增大氢离子浓度,从而增大反应速率,但硫酸的量增大,导致生成氢气的量增大,故A错误;
B.加入醋酸钠固体,醋酸钠和稀硫酸反应生成醋酸,酸最终电离出氢离子总量不变,且溶液中氢离子浓度减小,所以反应速率减小,故B错误;
C.升高温度,增大活化分子百分数,所以反应速率增大,但稀硫酸总量不变,所以生成氢气总量不变,故C正确;
D.钠和水或酸反应都生成氢气,所以增大氢气总量,故D错误;
故选C.
点评 本题考查化学反应速率影响因素,为高频考点,明确化学反应速率影响原理是解本题关键,注意题干中限制性条件,题目难度不大.

练习册系列答案
相关题目
13.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 65%的酒精用于消毒 | B. | Al(OH)3可用于治疗胃酸过多 | ||
| C. | 明矾用于水的杀菌消毒 | D. | 从海水中提取可燃冰 |
14.下列离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
11.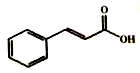 我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
 我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )
我市盛产荔技、荔枝核中的有机物3-苯基-2-丙烯酸(俗名肉桂酸)含量高达47%,结构如图所示.下列有关说法不正确的是( )| A. | 肉桂酸可使酸性高锰酸钾溶液褪色 | |
| B. | 肉桂酸能与银氨溶液发生银镜反应 | |
| C. | 肉桂酸分子式为C7H8O2 | |
| D. | 肉桂酸分子中至少有12个原子共平面 |
18.下列金属冶炼的方法错误的是( )
| A. | 加热分解Ag2O冶炼银 | B. | 用CO还原氧化铁冶炼铁 | ||
| C. | 钠与Mg2Cl溶液反应冶炼镁 | D. | 电解熔融氧化铝冶炼铝 |
8.下列化合物中,不含共价键的是( )
| A. | H2O | B. | NaOH | C. | MgCl2 | D. | CO2 |
12.A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序为( )
| A. | E、B、A、D、C | B. | D、B、C、A、E | C. | E、C、D、B、A | D. | A、B、C、D、E |
1.下列除去杂质的方法正确的是( )
| A. | 除去N2中少量的O2,通过灼热的CuO粉末,收集气体 | |
| B. | 除去CO2中少量的HCl,通入Na2CO3溶液,收集气体 | |
| C. | 除去KCl溶液中少量的MgCl2,加入足量的NaOH溶液,过滤 | |
| D. | 除去FeCl2溶液中少量的FeCl3,加入足量铁屑,充分反应后,过滤 |