题目内容
【题目】某化学兴趣小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1数据计算,用KMnO4的浓度变化表示反应速率 v(KMnO4)= 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图乙所示。 该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。
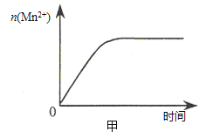
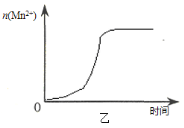
①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并选表中空白处应加入的物质。
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
4 | 3.0 | 2.0 | 3.0 | 2.0 |
| |
A.KMnO4 B.H2C2O4 C.K2SO4 D.MnSO4
③若该小组同学提出的假设成立,应观察到的现象是 。
【答案】(1)其他条件相同时,增大KMnO4浓度(或反应物浓度),反应速率增大
(2)1.5×10-2mol·L-1·min-1或0.015 mol·L-1·min-1
(3)①生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用) ②D
③实验4与实验1比较,溶液褪色所需时间短 或:溶液褪色所用时间(t)小于4min(或其他合理答案)
【解析】
试题分析:(1)从表中数据,可知改变的条件是KMnO4浓度,其他条件相同时,增大KMnO4浓度,褪色时间变短,则反应速率增大。
(2)草酸的物质的量为:0.6mol/L×0.003L=0.0018mol,高锰酸钾的物质的量为:0.2mol/L×0.003L=0.0006mol,草酸和高锰酸钾的物质的量之比为:0.0018mol:0.0006mol=3:1,显然草酸过量,高锰酸钾完全反应,混合后溶液中高锰酸钾的浓度为:![]() =0.06mol/L,这段时间内平均反应速率v(KMnO4)=0.06mol/L÷4min=1.5×10-2 mol/(Lmin)。
=0.06mol/L,这段时间内平均反应速率v(KMnO4)=0.06mol/L÷4min=1.5×10-2 mol/(Lmin)。
(3)①由图乙可知,反应开始后速率增大的比较快,说明生成物中的MnSO4(或Mn2+)为该反应的催化剂。
②与实验1作对比实验,则加入的硫酸锰的量不同,其它条件必须相同,所以加入的少量固体为MnSO4,答案选D。
③若该小组同学提出的假设成立,则反应速率加快,溶液褪色的时间小于4min,从而说明Mn2+是催化剂。

 名校课堂系列答案
名校课堂系列答案