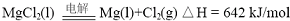题目内容
(2012?江苏一模)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.某工厂对制革工业污泥中Cr(Ⅲ)的工艺如下:
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.
(1)实验室用18.4mol?L-1的浓硫酸配制250mL 4.8mol?L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需
(2)酸浸时,为了提高浸取率可采取的措施有
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.滤液Ⅱ中阳离子主要有
(5)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是
(6)写出上述流程中用SO2进行还原的化学方程式

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.
(1)实验室用18.4mol?L-1的浓硫酸配制250mL 4.8mol?L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需
250mL容量瓶、胶头滴管
250mL容量瓶、胶头滴管
.(2)酸浸时,为了提高浸取率可采取的措施有
升高反应温度
升高反应温度
、增大固体颗粒的表面积
增大固体颗粒的表面积
.(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:
2Cr3++3H2O2+H2O=Cr2O72-+8H+
2Cr3++3H2O2+H2O=Cr2O72-+8H+
.(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | -- | -- | -- |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
Na+、Mg2+、Ca2+
Na+、Mg2+、Ca2+
;但溶液的pH不能超过8,其理由是pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用
pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用
.(5)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是
Ca2+、Mg2+
Ca2+、Mg2+
.(6)写出上述流程中用SO2进行还原的化学方程式
3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH
3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH
.分析:(1)依据溶液配制的步骤和过程分析所用到的仪器,主要仪器应有配制溶液的容量瓶和定容需要的胶头滴管;配置一定物质的量浓度的溶液所需的玻璃仪器有:烧杯、玻璃棒、吸量管、容量瓶和胶头滴管;
(2)酸浸时,为了提高浸取率可采取的措施是延长浸取时间、加快溶解速度等措施;硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+,酸浸是溶解物质为了提高浸取率,可以升高温度增大物质溶解度,增大接触面积增大反应速率,或加快搅拌速度等;
(3)根据双氧水的性质分析,双氧水有强氧化性,能氧化还原性的物质,依据氧化还原反应电子守恒、原子守恒配平书写离子方程式;
(4)硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.加入过氧化氢氧化铬离子为Cr2O72-,加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.
溶液PH=8,Fe3+、Al3+沉淀完全,滤液Ⅱ中阳离子主要Na+、Ca2+和Mg2+;超过PH=8,氢氧化铝是两性氢氧化物会溶解于强碱溶液中影响铬离子的回收利用;
(5)钠离子交换树脂交换 的离子是钙离子和镁离子.
(6)依据流程图中的转化关系和产物,结合二氧化硫的还原性,利用氧化还原反应原理分析书写.
(2)酸浸时,为了提高浸取率可采取的措施是延长浸取时间、加快溶解速度等措施;硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+,酸浸是溶解物质为了提高浸取率,可以升高温度增大物质溶解度,增大接触面积增大反应速率,或加快搅拌速度等;
(3)根据双氧水的性质分析,双氧水有强氧化性,能氧化还原性的物质,依据氧化还原反应电子守恒、原子守恒配平书写离子方程式;
(4)硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.加入过氧化氢氧化铬离子为Cr2O72-,加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.
溶液PH=8,Fe3+、Al3+沉淀完全,滤液Ⅱ中阳离子主要Na+、Ca2+和Mg2+;超过PH=8,氢氧化铝是两性氢氧化物会溶解于强碱溶液中影响铬离子的回收利用;
(5)钠离子交换树脂交换 的离子是钙离子和镁离子.
(6)依据流程图中的转化关系和产物,结合二氧化硫的还原性,利用氧化还原反应原理分析书写.
解答:解:(1)配置一定物质的量浓度的溶液所需的玻璃仪器有:烧杯、玻璃棒、吸量管、容量瓶和胶头滴管,故答案为:250mL容量瓶、胶头滴管;
(2)酸浸时,为了提高浸取率可采取的措施是:延长浸取时间、加快溶解速度等措施,
故答案为:升高反应温度;增大固体颗粒的表面积;
(3)双氧水有强氧化性,能氧化还原性的物质,Cr3+有还原性,Cr3+能被双氧水氧化为高价离子,以便于与杂质离子分离,
故答案为:2Cr3++3H2O2+H2O=Cr2O72-+8H+;
(4)硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.加入过氧化氢氧化铬离子为Cr2O72-,加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.
溶液PH=8,Fe3+、Al3+沉淀完全,滤液Ⅱ中阳离子主要Na+、Ca2+和Mg2+;超过PH=8,氢氧化铝是两性氢氧化物会溶解于强碱溶液中影响铬离子的回收利用;
故答案为:Na+、Mg2+、Ca2+;pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用;
(5)钠离子交换树脂交换的离子是钙离子和镁离子,故答案为:Ca2+、Mg2+;
(6)二氧化硫具有还原性,被滤液Ⅱ中通过离子交换后的溶液中Na2CrO4氧化为硫酸,Na2CrO4氧被还原为CrOH(H2O)5SO4,水溶液中生成氢氧化钠溶液和硫酸反应生成硫酸钠,依据原子守恒分析书写配平;3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH,
故答案为:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.
(2)酸浸时,为了提高浸取率可采取的措施是:延长浸取时间、加快溶解速度等措施,
故答案为:升高反应温度;增大固体颗粒的表面积;
(3)双氧水有强氧化性,能氧化还原性的物质,Cr3+有还原性,Cr3+能被双氧水氧化为高价离子,以便于与杂质离子分离,
故答案为:2Cr3++3H2O2+H2O=Cr2O72-+8H+;
(4)硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.加入过氧化氢氧化铬离子为Cr2O72-,加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.
溶液PH=8,Fe3+、Al3+沉淀完全,滤液Ⅱ中阳离子主要Na+、Ca2+和Mg2+;超过PH=8,氢氧化铝是两性氢氧化物会溶解于强碱溶液中影响铬离子的回收利用;
故答案为:Na+、Mg2+、Ca2+;pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用;
(5)钠离子交换树脂交换的离子是钙离子和镁离子,故答案为:Ca2+、Mg2+;
(6)二氧化硫具有还原性,被滤液Ⅱ中通过离子交换后的溶液中Na2CrO4氧化为硫酸,Na2CrO4氧被还原为CrOH(H2O)5SO4,水溶液中生成氢氧化钠溶液和硫酸反应生成硫酸钠,依据原子守恒分析书写配平;3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH,
故答案为:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.
点评:本题考查了离子方程式、化学方程式的书写、物质的分离等知识点,难度较大,注意会运用溶液的PH值对溶液中的离子进行分离,除杂的原则是:除去杂质且不引进新的杂质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
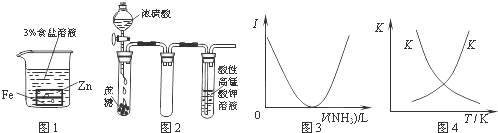


 ,则异蒲勒醇的结构简式为
,则异蒲勒醇的结构简式为
 的合成路线流程图.(无机试剂任用,合成路线流程图示例如下:
的合成路线流程图.(无机试剂任用,合成路线流程图示例如下: )
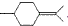
)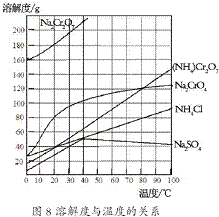 (2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:
(2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下: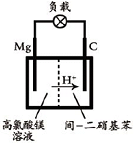 (2012?江苏一模)镁及其合金广泛应用于航空航天、交通、电池等行业,金属镁的制备方法主要有:
(2012?江苏一模)镁及其合金广泛应用于航空航天、交通、电池等行业,金属镁的制备方法主要有: