题目内容
11.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.(1)烟气脱硫、脱硝的环境意义是防止酸雨的发生.
(2)选择性催化还原法的脱硝原理为:6NOx+4x NH3 $\frac{\underline{\;催化剂\;}}{\;}$(3+2x)N2+6xH2O
①上述反应中每转移3mol电子,生成标准状况下N2的体积为$\frac{16.8+11.2x}{x}$L.
②已知:2H2(g)+O2(g)═2H2O (g)△H=-483.6kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
N2(g)+O2(g)═2NO(g)△H=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)═5N2(g)+6H2O(g)的△H=-724.5kJ•mol-1.
(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
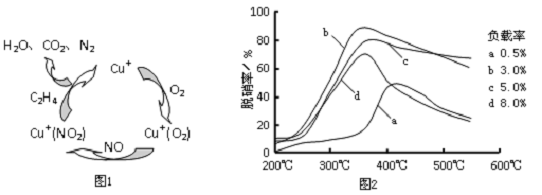
①写出该脱硝原理总反应的化学方程式:6NO+3O2+2C2H4$\frac{\underline{\;催化剂\;}}{\;}$3N2+4CO2+4H2O.
②为达到最佳脱硝效果,应采取的条件是350℃、负载率3%.
分析 (1)硫的氧化物、氮的氧化物是形成酸雨的主要成因,烟气脱硫、脱硝可以防止酸雨的发生;
(2)①反应中氨气中的N元素由-3价升高为0价,据此计算转移3mol电子参加反应的氨气的物质的量,再根据方程式计算生成的氮气,根据V=nVm计算氮气的体积;
②a、2H2(g)+O2(g)═2H2O (g)△H=-483.6kJ•mol-1
b、N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
c、N2(g)+O2(g)═2NO(g)△H=-180.5kJ•mol-1
依据盖斯定律计算,a×3-b×2-c×3得到反应的热化学方程式;
(3)①图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,据此写出反应的总方程式;
②为达到最佳脱硝效果,应满足脱硝率高,负载率低,适宜的温度.
解答 解:(1)烟气脱硫、脱硝可以降低硫的氧化物、氮的氧化物含量,防止酸雨的发生,
故答案为:防止酸雨的发生;
(2)①反应中氨气中的N元素由-3价升高为0价,化合价升高3价,泽尔转移3mol电子参加反应的氨气的物质的量为:$\frac{3mol}{3}$=1mol,根据方程式可知生成的氮气的物质的量为:1mol×$\frac{3+2x}{4x}$=$\frac{3+2x}{4x}$mol,
氮气的体积为:$\frac{3+2x}{4x}$mol×22.4L/mol=$\frac{16.8+11.2x}{x}$L,
故答案为:$\frac{16.8+11.2x}{x}$;
②a、2H2(g)+O2(g)═2H2O (g)△H=-483.6kJ•mol-1
b、N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
c、N2(g)+O2(g)═2NO(g)△H=-180.5kJ•mol-1
依据盖斯定律计算,a×3-b×2-c×3得到反应的热化学方程式为:6NO(g)+4NH3(g)═5N2(g)+6H2O(g)的△H=-724.5kJ•mol-1
故答案为:-724.5kJ•mol-1;
(3)①根据图1可知,在催化剂的作用下,C2H4与NO、O2反应最终生成N2、CO2、H2O,反应总方程式为:6NO+3O2+2C2H4$\frac{\underline{\;催化剂\;}}{\;}$3N2+4CO2+4H2O,
故答案为:6NO+3O2+2C2H4$\frac{\underline{\;催化剂\;}}{\;}$3N2+4CO2+4H2O;
②由图可知,b曲线的最高点处,脱硝率高,负载率低,温度温度适宜,适宜适合条件为350℃、负载率3%,
故答案为:350℃、负载率3%.
点评 本题以烟气的脱硫和脱硝为载体,考查环境保护、氧化还原反应计算、方程式书写等知识,题目难度中等,本题注意把握数据处理和图象分析.

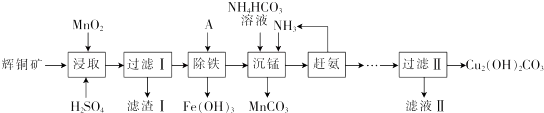
已知:①[Cu(NH3)4]SO4在常温下稳定,在热水中会分解生成NH3;
②部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol•L-1 计算):
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
(1)能加快浸取速率的措施有粉碎矿石、升高温度(或适当增加酸的浓度或搅拌).(任写2条)
(2)浸取后得到的浸出液中含有CuSO4、MnSO4.写出浸取时产生CuSO4、MnSO4反应的化学方程式:2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O,滤渣I的成分为 MnO2、SiO2和S.
(3)“除铁”的方法是通过调节溶液pH,使 Fe3+水解转化为Fe(OH)3,加入的试剂A可以是氨水(填化学式),调节溶液pH的范围为3.2≤PH<4.4.
(4)“沉锰”(除Mn2+)过程中发生反应的离子方程式为Mn2++HCO3-+NH3=MnCO3↓+NH4+,“赶氨”时,最适宜的操作方法为加热.
(5)测定碱式碳酸铜纯度町用滴定法:称取6.2500g样品于100ml_小烧杯中,加入20ml.蒸馏水搅拌,再加入8ml.6mol•L-1 硫酸使其完全溶解,冷却后定量转移至250mL容量瓶中,加水定容,摇匀,移取25.00mL配好的溶液于锥形瓶中,加入40.OO mL0.2000mol•L-1 EDTA溶液,然后加入指示剂,再用0.2000mol•L-1的Zn2+标准溶液滴定至终点,消耗标准溶液18.00mL.已知EDTA与Cu2+、Zn2+均按物质的量比1:1反应,则样品中的Cu2(OH)2CO3质量分数为.78.14%.
| A. | 1mol任何气体的体积约是22.4L | |
| B. | 标准状况下,1mol H2O 所占的体积约为22.4L | |
| C. | 常温常压下,1mol O2 所占的体积约为22.4L | |
| D. | 标准状况下,体积为22.4LN2 和N2O 的混合气体,其中约含有2mol N 原子 |
| A. | 纯盐酸、空气、硫酸、干冰 | B. | 蒸馏水、氨水、碳酸氢钠、二氧化硫 | ||
| C. | 胆矾、盐酸、铁、碳酸钙 | D. | 生石灰、浓硫酸、氯化铜、碳酸钠 |
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 化合物中各元 素原子个数比 | A:C=1:1 | A:B=1:1 | D:C=1:1 | E:F=1:3 | B:F=1:4 |
(2)向甲的水溶液中加入MnO2,氧化产物是O2(填化学式);已知有机物乙的分子为直线结构,乙的分子式为C2H2;
(3)若E单质可以与D的最高价氧化物的水化物溶液发生反应,请写出该反应化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(4)以E单质为阳极,在H2SO4溶液中电解,可以在E表面形成致密氧化膜保护E材料不被腐蚀,写出阳极电极反应式为2Al+3H2O-6e-=Al2O3+6H+.