题目内容
A、B、C、D四种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D为同一主族,C元素的价电子排布为ns2πp2n,D在空气中燃烧可以得到淡黄色固体。又知四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体。请回答下列问题:
(1)D在元素周期表中的位置是 。
(2)比较元素B和C的第一电离能:B C(填“大于”、“小于”或“不确定”),将BA3通入溴水中可发生反应,生成B的单质和一种盐Y,B的单质中的σ键和π键个数比为 ,盐Y的晶体类型是 。
(3)D与A形成的粒子个数比为1:1的简单化合物可与水反应生成A的单质,该反应的化学方程式为 。
(4)已知B2A4和过氧化氢混合可作火箭推进剂。12.8g液态B2A4与足量过氧化氢反应生成B的单质和气态水,放出256.65kJ的热量:
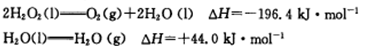
写出液态B2A4和氧气反应生成B的单质和液态A2C的热化学方程式 。
(1)D在元素周期表中的位置是 。
(2)比较元素B和C的第一电离能:B C(填“大于”、“小于”或“不确定”),将BA3通入溴水中可发生反应,生成B的单质和一种盐Y,B的单质中的σ键和π键个数比为 ,盐Y的晶体类型是 。
(3)D与A形成的粒子个数比为1:1的简单化合物可与水反应生成A的单质,该反应的化学方程式为 。
(4)已知B2A4和过氧化氢混合可作火箭推进剂。12.8g液态B2A4与足量过氧化氢反应生成B的单质和气态水,放出256.65kJ的热量:
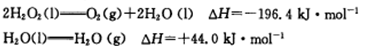
写出液态B2A4和氧气反应生成B的单质和液态A2C的热化学方程式 。
(1)第三周期IA族(2分)
(2)大于(2分) 2(2分) 离子晶体(2分)
(3)NaH+H2O=NaOH+H2↑ (2分)
(4)N2H4(l)+O2(g)=N2(g)+2H2O(l) △H="-621.2" kJ·mol-1(2分)
(2)大于(2分) 2(2分) 离子晶体(2分)
(3)NaH+H2O=NaOH+H2↑ (2分)
(4)N2H4(l)+O2(g)=N2(g)+2H2O(l) △H="-621.2" kJ·mol-1(2分)
试题分析:由D在空气中燃烧得到淡黄色固体可知D为Na,再结合A、D同主族以及四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体可知,A一定为H,再结合B的价电子排布可推知B、C分别为N、O。(2)因N的2p轨道处于半充满的稳定状态,故第一电离能大于同周期相邻的氧元素;由氧化还原反应规律可得到盐Y为NH4 Br,属于离子晶体,在单质N2中存在氮氮三键,其中1个σ键和2个π键。(3)NaH与H2O发生归中反应得到H2与NaOH。(4)利用题给信息可知:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-641.6kJ/mol,然后利用“盖斯定律”结合已知热化学方程式进行变形即可。

练习册系列答案
相关题目
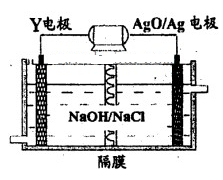
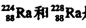 是中子数不同质子数相同的同种核素
是中子数不同质子数相同的同种核素

 2A(g) △H =-92.4 kJ?mol―1
2A(g) △H =-92.4 kJ?mol―1