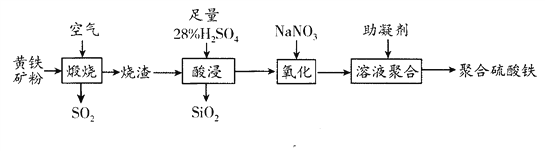
题目内容
【题目】如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 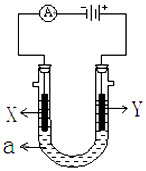
①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,(填X或Y)电极附近先变红色,X极上的电极反应式为 .
②若要在铁制品上镀一定厚度的Cu层,Y电极反应式为
③若X、Y都是铂电极,电解某金属M的氯化物(MCl2)溶液,当收集到11.2L氯气时(标准状况),阴极增重32g.该金属的相对原子质量是 .
【答案】X;2H++2e﹣=H2↑;Cu﹣2e﹣=Cu 2+;64
【解析】解:①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e﹣=H2↑,同时该电极附近有OH﹣生成,导致溶液碱性增强,滴入几滴酚酞试液会变红,
所以答案是:X;2H++2e﹣=H2↑;②若要在铁制品上镀一定厚度的Cu层,镀层作阳极、镀件作阴极,电解质溶液为含有铜离子的可溶性盐溶液,则Cu作阳极、Fe制品作阴极,Y为阳极,电极反应式为Cu﹣2e﹣=Cu 2+,
所以答案是:Cu﹣2e﹣=Cu 2+;③若X、Y都是铂电极,电解某金属M的氯化物(MCl2)溶液,当收集到11.2L氯气时(标准状况),n(Cl2)= ![]() =0.5mol,转移电子的物质的量=0.5mol×2=1mol,阴极增重32g,根据转移电子守恒知,阴极上转移1mol电子,MCl2中M化合价为+2价,要转移1mol电子,则析出0.5molM单质,该金属的摩尔质量=
=0.5mol,转移电子的物质的量=0.5mol×2=1mol,阴极增重32g,根据转移电子守恒知,阴极上转移1mol电子,MCl2中M化合价为+2价,要转移1mol电子,则析出0.5molM单质,该金属的摩尔质量= ![]() =64g/mol,金属单质的摩尔质量在数值上等于其相对原子质量,所以其相对原子质量为64,
=64g/mol,金属单质的摩尔质量在数值上等于其相对原子质量,所以其相对原子质量为64,
所以答案是:64.

【题目】I.下图是中学化学常用的实验装置,诮回答下列问题

(1)用图I进行物质的分离提纯,该分离方法为________,若利用装置I分离酒精和水的混合物,还缺少的仪器__________;①的名称是__________,②的进水口是________(填“f" 或“g”)。
(2)现需配制500mL、0.1mol/LKCl 溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处: ①_________;②____________。
(3)仪器①~④中,使用时必须检查是否漏水的是_________(填序号)。
Ⅱ.分离和提纯物质的方法不仅用于实验研究而且广泛应用于工业生产和生活实际。
(4)海水晒盐过程中,通过蒸发的方法可得到粗盐固体;再将粗盐固体溶解后,再用过滤的方法除去其中的泥沙。粗盐中除泥沙外还含有可溶性杂质(如下表所示),可按下表所示由上至下的顺序依次除去(将表格填写完整)。
杂质 | 加入试剂的化学式 | 发生反应的离子方程式 |
硫酸盐 | ___________ | ___________ |
MgCl2 | NaOH | ___________ |
CaCl2 | Na2CO3 | ___________ |
依次加入上述试剂后,完全反应后,再进行过滤,再加入适量的盐酸 可除去上述步骤引入的 杂质离子。
(5) 从海带中可提取碘单质。用萃取的方法可将碘单质从水溶液中提取出来,该方法利用了I2在不同溶剂中的_______性不同。