题目内容
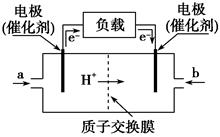
有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应式为2H2+O2===2H2O,负极反应为H2+CO -2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )
-2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )
 -2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )
-2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )| A.正极反应为2H2O+O2+4e-===4OH- | B.CO 向负极移动 向负极移动 |
| C.电子由正极经外电路流向负极 | D.电池中CO 的物质的量将逐渐减少 的物质的量将逐渐减少 |
B
试题分析:正极为还原反应,A错误,阴离子向负极移动,B正确,电子由负极出,正极入,C错误,总反应没有消耗CO32-,所以CO32-的物质的量不变,D错误。答案选B。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
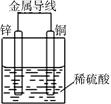
铜锌原电池工作时,下列叙述正确的是( )

A、正极反应为:Zn—2e-=Zn2+
B、B、在外电路中,电子从铜片流向锌片
C、电池反应为:Zn+Cu2+=Zn2+ +Cu
D、盐桥中的K+移向ZnSO4溶液

A、正极反应为:Zn—2e-=Zn2+
B、B、在外电路中,电子从铜片流向锌片
C、电池反应为:Zn+Cu2+=Zn2+ +Cu
D、盐桥中的K+移向ZnSO4溶液



 Li的质量是 g。
Li的质量是 g。