题目内容
在T℃时,向1L固定体积的密闭容器M中加入2mol X和1mol Y,发生如下反应:2X(g)+Y(g)?aZ(g)+W(g)△H=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小.请回答下列问题:
(1)化学计量数a的值为 .
(2)下列能说明该反应达到了化学平衡状态的是 (填序号).
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的分子数一定 d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是 kJ.
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则 (填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M N(填“>”、“<”或“=”).
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
若在某温度下,2mol X和1mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为 ℃.
(6)维持T℃温度不变,若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为 kJ.
(1)化学计量数a的值为
(2)下列能说明该反应达到了化学平衡状态的是
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的分子数一定 d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
(6)维持T℃温度不变,若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为
考点:化学平衡的计算,化学平衡状态的判断
专题:化学平衡专题
分析:(1)该反应是一个放热反应,升高温度平衡向逆反应方向移动,混合气体的平均相对分子质量减小,则气体反应物计量数之和大于气体生成物计量数之和;
(2)当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,以此解答该题;
(3)反应物的浓度不变,则其转化率不变,放出的热量不变;
(4)该条件下,恒压与恒容相比,相当于增大压强,增大压强平衡向正反应方向移动,压强越大,反应速率越大,据此判断到达平衡时间,根据平衡移动方向判断X的质量分数;
(5)计算该温度下的平衡常数,根据表格中平衡常数和温度的关系判断;
(6)根据减少的分子数计算参加反应的X的物质的量,根据X和反应热之间的关系式计算.
(2)当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,以此解答该题;
(3)反应物的浓度不变,则其转化率不变,放出的热量不变;
(4)该条件下,恒压与恒容相比,相当于增大压强,增大压强平衡向正反应方向移动,压强越大,反应速率越大,据此判断到达平衡时间,根据平衡移动方向判断X的质量分数;
(5)计算该温度下的平衡常数,根据表格中平衡常数和温度的关系判断;
(6)根据减少的分子数计算参加反应的X的物质的量,根据X和反应热之间的关系式计算.
解答:
解:(1)该反应是一个放热反应,升高温度平衡向逆反应方向移动,混合气体的平均相对分子质量减小,则气体反应物计量数之和大于气体生成物计量数之和,所以a=1,故答案为:1;
(2)a、由于反应前后气体的化学计量数之和不相等,则平衡时压强不再发生变化,故a正确;
b、由于是在固定体积的容器中反应,则无论是否达到平衡状态,密度都不变,故b错误;
c、反应达到平衡状态时,物质的浓度、含量、质量等不再发生变化,则平衡时容器内Z分子数一定,故c正确;
d、反应物和生成物都是气体,无论是否达到平衡状态,容器内气体的质量都一定,故d错误.
故答案为:ac;
(3)若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),X和Y的浓度不变,所以其转化率不变,该反应达到平衡状态时,放出的热量不变为Q1,故答案为:Q1;
(4)该条件下,恒压与恒容相比,相当于增大压强,压强越大,反应速率越大,反应到达平衡的时间越短,增大压强平衡向正反应方向移动,则X的质量发生越小,
故答案为:N;>;
(5)2mol X和1mol Y在容器M中反应并达到平衡,x的平衡转化率为50%,则平衡时,c(X)=
=1mol/L,C(Y)=
=0.5mol/L,c(Z)=c(W)=
=0.5mol/L,k=
=0.5,所以其温度是350℃,故答案为:350℃.
(6)同一容器中,物质的分子数之比等于物质的量之比,当反应达到平衡时容器内的分子数目减少10%时,气体的物质的量减少10%,即气体的物质的量减少(4+6)mol×10%=1mol,根据2X(g)+Y(g) ?Z(g)+W(g)知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,则反应中放出的热量为QkJ,故答案为:Q;
?Z(g)+W(g)知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,则反应中放出的热量为QkJ,故答案为:Q;
(2)a、由于反应前后气体的化学计量数之和不相等,则平衡时压强不再发生变化,故a正确;
b、由于是在固定体积的容器中反应,则无论是否达到平衡状态,密度都不变,故b错误;
c、反应达到平衡状态时,物质的浓度、含量、质量等不再发生变化,则平衡时容器内Z分子数一定,故c正确;
d、反应物和生成物都是气体,无论是否达到平衡状态,容器内气体的质量都一定,故d错误.
故答案为:ac;
(3)若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),X和Y的浓度不变,所以其转化率不变,该反应达到平衡状态时,放出的热量不变为Q1,故答案为:Q1;
(4)该条件下,恒压与恒容相比,相当于增大压强,压强越大,反应速率越大,反应到达平衡的时间越短,增大压强平衡向正反应方向移动,则X的质量发生越小,
故答案为:N;>;
(5)2mol X和1mol Y在容器M中反应并达到平衡,x的平衡转化率为50%,则平衡时,c(X)=
| (1-50%)×2mol |
| 1L |
1mol-1mol×
| ||
| 1L |
| ||
| 1L |
| 0.5×0.5 |
| 0.5×12 |
(6)同一容器中,物质的分子数之比等于物质的量之比,当反应达到平衡时容器内的分子数目减少10%时,气体的物质的量减少10%,即气体的物质的量减少(4+6)mol×10%=1mol,根据2X(g)+Y(g)
 ?Z(g)+W(g)知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,则反应中放出的热量为QkJ,故答案为:Q;
?Z(g)+W(g)知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,则反应中放出的热量为QkJ,故答案为:Q;
点评:本题考查的化学平衡的有关知识,明确化学平衡状态的判断方法、等效平衡、化学平衡的影响因素等知识点,注意恒容条件下,向体系中通入惰性气体是否影响平衡移动,为易错点.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列说法不正确的是( )
| A、某烷烃主链4个碳原子数的同分异构体有2种,则与其碳原子个数相同的且主链4个碳原子的单烯烃有4种 |
| B、(CH3)2C(OH)CH2CH3的名称为:2-甲基-2-羟基丁烷 |
C、1mol有机物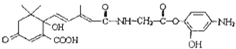 与NaOH溶液反应,最多消耗5mol NaOH 与NaOH溶液反应,最多消耗5mol NaOH |
D、1mol β-紫罗兰酮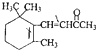 与1mol Br2发生加成反应可得到3种不同产物 与1mol Br2发生加成反应可得到3种不同产物 |
有机物A是有机合成的中间体,其结构简式为 ,有关说法错误的是( )
,有关说法错误的是( )
 ,有关说法错误的是( )
,有关说法错误的是( )| A、分子式为C13H18O2 |
| B、含有醛基、羟基等官能团 |
| C、1mol该有机物能与3mol H2加成反应 |
| D、能使高锰酸钾溶液褪色也能使溴水褪色 |
 如图是某同学利用注射器设计的简易实验装置.甲管中注入10mL
如图是某同学利用注射器设计的简易实验装置.甲管中注入10mL 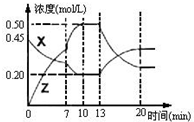 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应