题目内容
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.1mol![]() 发生氧化还原反应时,转移的电子数目一定为2NA
发生氧化还原反应时,转移的电子数目一定为2NA
B.向含有1mol![]() 的溶液中通入足量的氯气完全反应时,转移的电子数目为2NA
的溶液中通入足量的氯气完全反应时,转移的电子数目为2NA
C.常温常压下,14g由![]() 与
与![]() 组成的混合气体含有的原子数目为NA
组成的混合气体含有的原子数目为NA
D.![]() 的浓硫酸与足量铜在加热条件下反应,生成
的浓硫酸与足量铜在加热条件下反应,生成![]() 分子的数目为0.46NA
分子的数目为0.46NA
【答案】C
【解析】
A.当过氧化钠发生歧化反应时,例如和水或二氧化碳反应,每mol过氧化钠只转移1mol电子,A项错误;
B.氯气具有强氧化性,可以将![]() 氧化成
氧化成![]() ,将2个
,将2个![]() 氧化成
氧化成![]() ,当氯气过量时,转移的电子数为3mol,B项错误;
,当氯气过量时,转移的电子数为3mol,B项错误;
C.质量与条件无关,氮气和一氧化氮的分子量均为28,则由![]() 算出气体的物质的量,二者都是双原子分子,因此一共有1mol原子,C项正确;
算出气体的物质的量,二者都是双原子分子,因此一共有1mol原子,C项正确;
D.该反应需要浓硫酸才能反应,当硫酸浓度变稀后反应即停止,因此无法计算生成的![]() 的量,D项错误;
的量,D项错误;
答案选C。

【题目】“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某化学研究性学习小组在实验室制备NaClO溶液,并进行性质探究和成分测定。
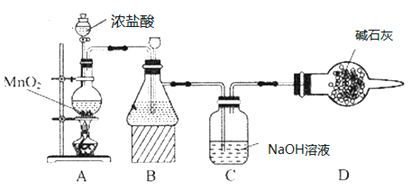
(1)该学习小组按如图装置进行实验(部分夹持装置省去),反应一段时间后,分别取B、C瓶中的溶液进行实验,实验现象如下表。
实验步骤 | 实验现象 | |
B瓶 | C瓶 | |
实验1:取样,滴加紫色石蕊试液 | 变红,不褪色 | 变蓝,不褪色 |
实验2:测定溶液的pH | 3 | 12 |
已知:①饱和NaClO溶液pH为11;②25°C时,弱酸电离常数为:H2CO3:K1=4.4×10-7,K2=4.7×10-11;HClO:K=3×10-8。回答下列问题:
①装置B盛装的试剂是___________,装置A中发生反应的离子方程式__________。
②C瓶溶液中的溶质是NaCl、__________(填化学式)。
③若将C瓶溶液换成NaHCO3溶液,按上述操作步骤进行实验,C瓶现象为:实验1中紫色石蕊试液立即褪色;实验2中C瓶溶液的pH=7。结合平衡移动原理解释紫色石蕊试液立即褪色的原因______
(2)测定C瓶溶液中NaClO含量(单位:g/L)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000mol/LNa2S2O3标准溶液滴定锥形瓶中的溶液,淀粉溶液显示终点后,重复操作2~3次,Na2S2O3溶液的平均用量为24.00mL。(已知:I2+2S2O32-=2I-+S4O62-)
①步骤I的锥形瓶中发生反应的离子方程式为_________。
②滴定至终点的现象_____________。
③C瓶溶液中NaClO含量为______g/L(保留2位小数)
【题目】合成气的主要成分是一氧化碳和氢气,可用于合成甲醇、二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1 kJ/mol
CO(g)+3H2(g) △H1=+206.1 kJ/mol
②CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H2=+247.3 kJ/mol
2CO(g)+2H2(g) △H2=+247.3 kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图所示:

则反应前5min的平均反应速率v(H2)=______。10min时,改变的外界条件可能是_______(填代号)。
A.压缩体积 B.增大体积 C.升高温度 D.加入催化剂
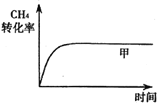
(2)如图所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。
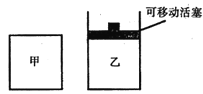
已知甲容器中CH4的转化率随时间变化的图像如图所示,请在图中画出乙容器中CH4的转化率随时间变化的图像_______。
(3)反应③中△H3=________。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见表:
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
此时反应③中正、逆反应速率的关系式是________(填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(4)800K时向下列三个密闭容器中各充入2 mol H2、1 mol CO,发生反应:2H2(g)+CO(g)CH3OH(g) △H<0,若三容器初始体积相同,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
甲. 乙.
乙. 丙.
丙.
①达到平衡时,平衡常数K(甲)________K(乙);K(乙)________K(丙)(填“>”、“<”或“=”)。
②达到平衡时H2的浓度c(H2)(甲)________c(H2)(乙);c(H2)(乙)________c(H2)(丙)(填“>”、“<”或“=”)。
(5)在以甲醇为燃料的电池中,电解质溶液为碱性,负极的电极反应式为_________,甲醇应用于燃料电池比甲醇直接用作燃料燃烧的优点是_______(回答一条即可)。