题目内容
【题目】1L 0.1mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是( )
A.电解质AgNO3溶液的浓度变为0.08mol/L
B.阳极上产生112mLO2(标况)
C.转移1.204×1022个电子
D.反应中有0.01mol的Ag被氧化
【答案】C
【解析】解:1L0.1mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,阳极反应式为Ag﹣e﹣=Ag+、阴极反应式为 Ag++e﹣=Ag,所以该装置是电镀池,A.因为溶解的Ag和析出的Ag质量相等,所以电解质溶液浓度不变,仍然为1mol/L,故A错误;
B.较活泼金属作阳极,阳极上金属失电子,所以阳极反应式为Ag﹣e﹣=Ag+ , 故B错误;
C.根据Ag﹣e﹣=Ag+知,析出2.16gAg时转移电子数= ![]() =1.204×1022 , 故C正确;
=1.204×1022 , 故C正确;
D.反应中被氧化n(Ag)= ![]() =0.02mol,故D错误;
=0.02mol,故D错误;
故选C.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
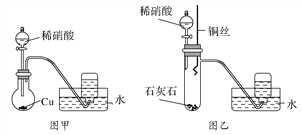
【题目】用如图所示装置进行下列实验,将分液漏斗中溶液X加入圆底烧瓶中与Y反应,对试管B中现象描述不正确的是

选项 | X溶液 | 固体Y | Z溶液 | 现象 |
A | 70%H2SO4 | Na2SO3溶液 | H2S溶液 | 产生浑浊 |
B | 浓氨水 | CaO | 酚酞试剂 | 溶液变红 |
C | 盐酸 | 大理石 | Na2SiO3溶液 | 出现白色沉淀 |
D | 浓盐酸 | MnO2 | NaOH溶液 | 黄绿色气体被吸收 |
A. A B. B C. C D. D