题目内容
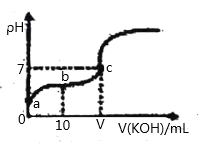
【题目】将含有0.4 mol CuSO4和0.1 mol NaCl的水溶液用惰性电极电解一段时间后,若在一个电极上得到6.4g Cu,则另一电极上生成气体(在标准状况)的体积为
A.1.12 LB.1.68 LC.2.24 LD.3.36L
【答案】B
【解析】
电解CuSO4和NaCl混合溶液时,阴极上Cu2+先放电,然后H+放电,阳极上Cl-先放电,然后OH-放电,若在一个电极上得到6.4g的Cu,其物质的量是6.4g÷64g/mol=0.1mol<0.4mol,说明Cu未反应完全,反应转移电子的物质的量是0.1mol×2=0.2mol,阳极上0.1molCl-放电,2Cl--2e-=Cl2↑,Cl-转移电子的物质的量=0.1mol×1=0.1mol<0.2mol,因此阳极上还有OH-离子放电,转移0.1mol电子,4OH--4e-=2H2O+O2↑,转移0.1mol电子生成O2的物质的量是n(O2)=![]() n(e-)=
n(e-)=![]() ×0.1mol=0.025mol,产生Cl2的物质的量n(Cl2)=
×0.1mol=0.025mol,产生Cl2的物质的量n(Cl2)=![]() ×0.1mol=0.05mol,所以反应产生气体的物质的量是0.05mol+0.025mol=0.075mol,则产生气体在标准状况的体积V=0.075mol×22.4L/mol=1.68L,故合理选项是B。
×0.1mol=0.05mol,所以反应产生气体的物质的量是0.05mol+0.025mol=0.075mol,则产生气体在标准状况的体积V=0.075mol×22.4L/mol=1.68L,故合理选项是B。

【题目】能源是人类赖以生存的基础。回答下列问题:
(1)下列不属于新能源的是________(填字母)。
a.煤炭 b.太阳能 c.风能 d.地热能
(2)已知:
Ⅰ.H2(g)+![]() O2(g)=H2O(g) H1=-241.8kJmol-1
O2(g)=H2O(g) H1=-241.8kJmol-1
Ⅱ.H2(g)+![]() O2(g)=H2O(l) H2=-285.8kJmol-1
O2(g)=H2O(l) H2=-285.8kJmol-1
气态分子中的化学键 | 断开1 mol化学键所需的能量/kJ |
O-H | 465 |
O=O | 498 |
①氢气的燃烧热为________kJmol-1.
②断开1 mol H-H键需要吸收的能量为________kJ。
③36 g H2O(1)完全分解生成氧气和氧气,需要吸收________kJ的能量。
(3)金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,反应中放出的热量如图所示。
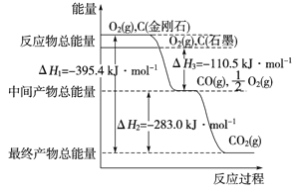
①在通常状况下,金刚石和石墨的稳定性较大的是________ (填“金刚石”或“石墨”)。
②12 g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为________kJ。