题目内容
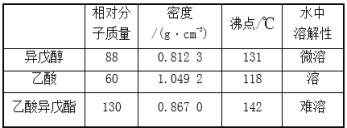
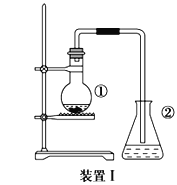
【题目】文献表明:工业上,向炽热铁屑中通入HCl生产无水FeCl2;相同条件下,草酸根(C2O42-)的还原性强于Fe2+。某化学研究性小组进行以下实验检验这一结论并测定三草酸合铁酸钾晶体[K3Fe(C2O4)3xH2O]中草酸根含量和结晶水含量。用如图所示装置制取无水FeCl2
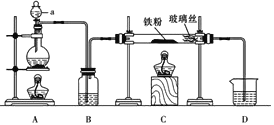
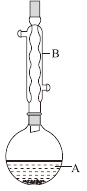
(1)仪器a的名称为____,B中的试剂为________。
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是________。
(3)若用D的装置进行尾气处理,存在的问题是________、________。
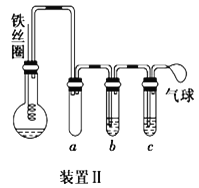
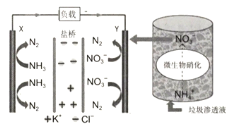
(4)某小组设计使用如图装置直接比较Fe2+和C2O42-的还原性强弱,并达到了预期的目的。

左池石墨电极为___极,写出右池电极反应式:________。
(5)为测定三草酸合铁酸钾晶体中草酸根的含量和结晶水的含量,进行了如下实验:
滴定过程:①称量mg三草酸合铁酸钾晶体样品,配制成250mL溶液
②取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液滴定,恰好消耗VmLamolL-1KMnO4溶液。C2O42-被全部转化的现象是___。
③该晶体中C2O42-的质量分数为___。
误差若盛放酸性KMnO4溶液的滴定管未用标准液润洗,会使结晶水x的数值___。(填“偏高”“偏低”“无影响”)
【答案】分液漏斗 浓硫酸 用HCl排尽装置中的空气,防止铁被氧化,使产品不纯 发生倒吸 可燃性气体H2不能被吸收 正 C2O422e=2CO2↑ 溶液由无色转变为浅紫红色,且半分钟内不再变化 ![]() 偏低
偏低
【解析】
由装置图可知,C中Fe与HCl反应生成FeCl2和H2,则A中产生HCl气体,可用氯化钠固体和浓硫酸加热反应制取HCl气体,用浓硫酸干燥气体,B中装浓硫酸,因加热时铁粉易被空气中的氧气氧化,且反应生成氢气,因此先点燃A处酒精灯排尽装置中的空气,再点燃C处的酒精灯,尾气是剩余的HCl气体和H2,HCl气体易溶于水导气管直接插入D中会引起倒吸。
(1)仪器a的名称为分液漏斗,B中的试剂为浓硫酸,可干燥HCl气体;
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是用HCl排尽装置中的空气,防止铁被氧化,使产品不纯;
(3)若用D的装置进行尾气处理,存在的问题是发生倒吸、可燃性气体H2不能被吸收;
(4)草酸根(C2O42)的还原性强于Fe2+可知,图中左侧铁离子得到电子,右侧草酸根离子失去电子,则左侧石墨电极为正极,右池电极反应式为C2O422e=2CO2↑;
(5)C2O42被全部转化的现象是溶液由无色转变为浅紫红色,且半分钟内不再变化,由5C2O42+2MnO4+16H+═2Mn2++10CO2↑+8H2O可知,晶体中C2O42的质量分数为: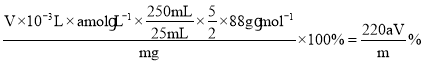 ,盛放酸性KMnO4溶液的滴定管未用标准液润洗,消耗高锰酸钾体积偏大,导致测定C2O42的含量偏大,则会使结晶水x的数值偏低。
,盛放酸性KMnO4溶液的滴定管未用标准液润洗,消耗高锰酸钾体积偏大,导致测定C2O42的含量偏大,则会使结晶水x的数值偏低。

 字词句段篇系列答案
字词句段篇系列答案