题目内容
【题目】为更有效处理工业废气中排放的氮氧化物(NOx)、SO2等,减少大气污染。科学家不断对相关反应进行研究尝试。
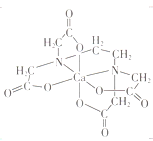
(1)脱硝反应机理如图,Cu+的作用是____________,C2H4参与的反应方程式 ______________ 。
(2) 选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g);ΔH= -1627 kJmol-1
4N2(g)+6H2O(g);ΔH= -1627 kJmol-1
① 其中被NO和O2氧化的NH3的比例 ________ 。
②该方法应控制反应温度在315~400℃之间,反应温度不宜过高的原因是________ 。
③ 氨氮比 n(NH3)/n(NO) 会直接影响该方法的脱硝率。如图为350 ℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 n(NH3)/n(NO) >1.0时,烟气中NO含量反而增大,主要原因是_________________________________。

(3) 烟气脱硫、脱硝一体化技术是大气污染防治研究的热点。ClO2及NaClO2均是性能优良的脱硫脱硝试剂。
① ClO2在酸性条件下稳定,在NaOH溶液中可歧化为NaClO3和NaClO2,该反应的化学方程式为____。

② 某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是________;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是________。
【答案】催化剂 2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+ 2:1 正反应放热,温度过高会降低NO的转化率 NH3和O2再次反应生成NO(或4NH3+5O2=4NO+6H2O) 2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O pH<7时,随着pH值的增大,ClO2的稳定性降低氧化性减弱,SO2的脱除率降低。 当pH>7.8后,随着碱性的增强,生成ClO2-增多,氧化性增强,SO2的脱除率上升
【解析】
(1) Cu+在反应前后不变为催化剂;用乙烯进行脱硝(NO),从图示可以知道,乙烯被氧化成二氧化碳;
(2)①根据得到电子的比例计算;
②根据温度对速率和化学平衡的影响分析;
③根据过量氨气与氧气的反应的产物分析;
(3)① ClO2在NaOH溶液中可歧化为NaClO3和NaClO2,根据得失电子守恒写出该反应的化学方程式;
②由图可知,当3<pH<7时,随pH的增大,ClO2的稳定性降低,氧化性减弱,SO2脱除率逐渐降低;在pH约7.8之后,随pH的增大,生成ClO2-增多,氧化性增强,SO2脱除率又开始升高。
(1) 催化剂在化学反应前后性质、质量不变,图示中Cu+在反应前后不变,为催化剂;用乙烯进行脱硝(NO),从图示可以知道,乙烯被NO氧化成二氧化碳(其中C由-2→+4),NO自身被还原成N2(其中N由+2→0),反应方程式为:2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+,
因此,本题正确答案是:催化剂;2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+;
(2)①由方程式4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)可知,该反应O2和NO都作氧化剂,1molO2得4mol电子,4molNO得8mol电子,因此被NO和O2氧化的NH3的比例为2:1,
4N2(g)+6H2O(g)可知,该反应O2和NO都作氧化剂,1molO2得4mol电子,4molNO得8mol电子,因此被NO和O2氧化的NH3的比例为2:1,
因此,本题正确答案是:2:1;
②该方法应控制反应温度在315~400℃之间,反应温度不宜过高,温度过高,使脱硝的主要反应的平衡向逆方向移动,脱硝率降低,
因此,本题正确答案是:正反应放热,温度过高会降低NO的转化率;
③当 n(NH3)/n(NO) >1.0时,过量的氨气与氧气反应生成NO,所以烟气中NO浓度增大,
因此,本题正确答案是:NH3和O2再次反应生成NO;
(3)① ClO2在NaOH溶液中可歧化为NaClO3和NaClO2,反应的化学方程式为2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O,
因此,本题正确答案是:2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O;
②由图可知,当3<pH<7时,随pH的增大,ClO2的稳定性降低,氧化性减弱,SO2脱除率逐渐降低;在pH约7.8之后,随pH的增大,生成ClO2-增多,氧化性增强,SO2脱除率又开始升高。
因此,本题正确答案是:pH<7时,随着pH值的增大,ClO2的稳定性降低氧化性减弱,SO2的脱除率降低;当pH>7.8后,随着碱性的增强,生成ClO2-增多,氧化性增强,SO2的脱除率上升。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室用密度1.18g/mL、质量分数为36.5%的浓盐酸配制250mL0.1mol/L的盐酸,回答下列问题:
(1)配制250mL0.1mol/L的盐酸
应量取的浓盐酸的体积/mL | 应选用的容量瓶的规格/mL | 除容量瓶外需要的其他仪器 |
____ | ____ | ____ |
(2)配制时,正确的操作顺序是____(填编号)。
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3 次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入适量蒸馏水,用玻璃棒搅拌, 使其混合均匀
C.将已冷却的溶液沿玻璃棒注入所选容量瓶中
D.盖好瓶塞,上下颠倒摇匀
E 改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm 处
(3)操作A中,将洗涤液都注入容量瓶,其目的是______, 若无操作A,则所配溶液浓度____(填“偏大”、“偏小”或“不变”)
(4)E中加蒸馏水不慎超过了刻度线,则所配溶液浓度____(填“偏大”、“偏 小”或“不变”),应如何处理______。