题目内容
【题目】NaCl是我们生活中必不可少的物质。将NaCl固体溶于水,溶解过程如图所示,下列说法正确的是
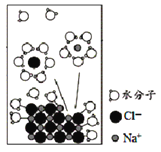
A.该过程发生了分解反应
B.离子从固体表面脱离后不会再回到固体表面
C.水合Na+的图示不科学
D.NaCl溶于水后发生了电离,是在通电条件下进行的
【答案】C
【解析】
A.该过程只有化学键的断裂,并没有新化学键的形成,不属于化学变化,更不是分解反应,故A错误;
B.该过程中存在两个过程:一方面在水分子作用下钠离子和氯离子脱离氯化钠的表面溶入水中,另一方面溶液中钠离子和氯离子受氯化钠表面阴、阳离子的吸引回到氯化钠的表面,最终会出现动态平衡NaCl(s)Na+(aq)+Cl-(aq),离子从固体表面脱离后会回到固体表面,故B错误;
C.钠离子带正电荷,形成水合离子时应该是水中带负电的氧原子靠近钠离子,即图示错误,故C正确;
D.NaCl溶于水后在水分子的作用下离子键断裂,形成水合离子,并不需要通电,故D错误;
故答案为C。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目