题目内容
【题目】铝电池性能优越,Al-Ag2O2电池用于电解尿素[CO(NH2)2]的碱性溶液制备氢气(隔膜Ⅱ仅阻止气体通过,a、b均为惰性电极)。下列说法正确的是( )
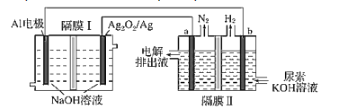
A.Ag电极是正极,反应后该电极区溶液pH减小
B.原电池的总反应为:2Al+3Ag2O2+2NaOH═2NaAlO2+3Ag2O+H2O
C.每消耗2.7g铝,理论上a、b两极共产生气体3.36L(标准状况)
D.a电极上的电极反应为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O
【答案】D
【解析】
A、Al-Ag2O2电池工作时,Al失去电子、被氧化、为负极,Ag2O2/Ag电极为正极,Ag2O2发生还原反应生成Ag,反应后该电极区pH增大,而不是减小,故A错误;
B、Al-Ag2O2电池工作时,Al失去电子、被氧化、为负极,Ag2O2/Ag电极为正极,Ag2O2发生还原反应生成Ag,则原电池的总反应方程式错误,故B错误;
C、2.7g的铝物质的量为:0.1mol,所以整个电路转移电子的物质的量为0.3mol,又a电极反应式为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O,b电极反应式为:2H++2e-═H2↑,所以生成氮气的物质的量为0.05mol,氢气的物质的量为:0.15mol,所以上a、b两级共产生气体0.2mol,标况下体积为:4.48L,而不是3.36L,故C错误;
D、a电极上尿素[CO(NH2)2]发生氧化反应,生成氮气和碳酸根离子,电极反应式为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O,故D正确;
答案选D。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】化合物A、B是中学常见的物质,其阴阳离子可从表中选择.
阳离子 | K+、Na+、NH4+、Fe2+、Ba2+、Cu2+ |
阴离子 | OH﹣、I﹣、NO3﹣、AlO2﹣、HCO3﹣、HSO4﹣ |
(1)若A的水溶液为无色,B的水溶液呈碱性,A、B的水溶液混合后,只产生不溶于稀硝酸的白色沉淀及能使湿润的红色石蕊试纸变蓝的气体,则:
①A中的化学键类型为_________(填“离子键”、“共价键”).
②A、B溶液混合后加热呈中性,该反应的离子方程__________________________ .
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则:
①A的化学式为__________________________ .
②经分析上述过程中溶液变黄的原因可能有两种(请用文字叙述)
Ⅰ._______________________.Ⅱ._________________________.
③请用一简易方法证明上述溶液变黄的原因_________________________.
④利用上述过程中溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为_.