��Ŀ����
����Ŀ��SF6��������ѹ�����豸�еġ������Ե���ء�����S(g)��F2(g)�Ʊ�SF6(g)�������仯��ͼ��ʾ������˵����ȷ����
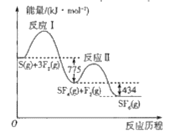
A.����֪S��F���ļ������ȷ��F��F���ļ���
B.S(g)��3F2(g)=SF6(g)��H=��1209kJ��mol��1
C.��S(g)��3F2(g)=SF6(g)��ȣ�S(s)��3F2(g)=SF6(g)�ų��������϶�
D.���ڷ�Ӧ��ų����������ڷ�Ӧ�����Է�Ӧ���ʣ���>��
���𰸡�A
��������
A�����ݵڶ����ķ�Ӧ�ȿ��Եó���![]() ��������֪S��F���ļ������ȷ��F��F���ļ��ܣ�A��ȷ��
��������֪S��F���ļ������ȷ��F��F���ļ��ܣ�A��ȷ��
B����ͼ�п�֪�÷�ӦΪ���ȷ�Ӧ��S(g)��3F2(g)=SF6(g)��H=-1209kJ��mol��1��B����
C����S(g)��S(s)�Ĺ����Ƿ��ȵģ�����S(g)��3F2(g)=SF6(g)��ȣ�S(s)��3F2(g)=SF6(g)�ų����������٣�C����
D�����ڷ�Ӧ���ų����������ڷ�Ӧ�������Ƿ�Ӧ�����뷴Ӧ�ȵĴ�С�أ����뷴Ӧ�Ļ���йأ�һ����ԽС��Ӧ����Խ�죬�ʷ�Ӧ����Ӧ������<����D����
�ʴ�Ϊ��A��

����Ŀ���ڻ�ѧ����Χ��Ũ����Ļ�ѧ���ʽ���������ʵ��̽���������������Ƿ����ձ��У����뼸��ˮ��������ȣ�Ȼ�����Ũ���ᣬ���ɺ�ɫ���ʡ�
��ش��������⣺
��1�����ɵĺ�ɫ����(����)��_____(�ѧʽ)��
��2�����ֺ�ɫ���ʼ�����Ũ�������û�����������壬����һ�������д̼�����ζ���Ǵ�������Ҫ��Ⱦ��֮һ�����ִ̼�����ζ������ɷ���_______(�ѧʽ)����Ӧ�Ļ�ѧ����ʽΪ_________��
��3����������Ũ���ᷴӦ��ʵ������˵��Ũ�������___________(�����)��
A������ | B����ˮ�� | C����ˮ�� | D��ǿ������ |
��4������2���в������д̼�����ζ������ͨ��Ʒ����Һ�У����Կ���Ʒ����Һ_______��˵�������������_______�ԣ�����2���в������д̼�����ζ������ͨ��ˮ�п�����һ�ֲ��ȶ����ֽ���ᣬ��д���÷�Ӧ�Ļ�ѧ����ʽ��__________________________________________��
��5���ܷ��ó���ʯ��ˮ�������������壿_______(������������������)�������ܣ�����д�����ܼ�����Լ�____________��
����Ŀ������β���к���CO��NOx����Ⱦ���������β����Ⱦ����Ҫ�о����⡣
(1)��֪�� N2(g) + O2(g)==2NO(g) ��H=+ 180.5kJ��mol-1
2C(s)+ O2(g)== 2CO(g) ��H= - 221.0kJ��mol-1
C(s)+ O2(g)==CO2(g) ��H= -393.5 kJ��mol-1
2CO(g)+ 2NO(g)== N2(g)+ 2CO2(g) ��H=_______kJ��mol-1
(2)ij�¶��£�Ϊ̽��2CO(g)+ 2NO(g)N2(g)+ 2CO2(g)�ķ�Ӧ���ʣ������崫������ò�ͬʱ���CO��NOŨ�����±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO)/10-4mol��L-1 | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
c(NO)/10-4mol��L-1 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
��ǰ2s�ڣ�������Ӧ��ƽ����Ӧ����v(NO)=_______��
�ڸ��¶��£�������Ӧ��ƽ�ⳣ��K=_________��
�۶���������Ӧ������������ȷ����________(����ĸ)��
A.��Ӧ�ڵ��������Է����� B.��2v��(CO)=v��(N2)ʱ����Ӧ�ﵽƽ��״̬
C.�о���Ӧ�ĸ�Ч���������ش� D.��Ӧ�ﵽƽ��ʱ��CO��NO��ת�������
(3)COŨ�ȷ�������ȼ�ϵ��Ϊ����ԭ������װ����ͼ��ʾ���õ���е����Ϊ������-�����ƣ�����O2-�����ڹ������NASICON�������ƶ���д����缫a�ĵ缫��Ӧʽ��_________��