题目内容
【题目】下列表示物质结构的化学用语或模型正确的是
A. 苯分子的比例模型:
B. CO2的电子式:![]()
C. Cl-离子的结构示意图:
D. 乙烯的结构式:CH2=CH2
【答案】A
【解析】
A.苯分子中存在6个C和6个H,其分子中所有原子共平面,苯的碳碳键为一种完全相同的独特键,苯的比例模型为:![]() ,故A正确;
,故A正确;
B.二氧化碳为共价化合物,分子中存在两个碳氧双键,氧原子和碳原子的最外层都达到8电子稳定结构,二氧化碳正确的电子式为:![]() ,故B错误;
,故B错误;
C.氯离子核电荷数为17,最外层电子数为8,氯离子的结构示意图为:![]() ,故C错误;
,故C错误;
D.乙烯分子中存在1个碳碳双键和4个碳氢键,乙烯的电子式为:![]() ,其结构式中需要用短线表示出所有的共价键,乙烯正确的结构式为:
,其结构式中需要用短线表示出所有的共价键,乙烯正确的结构式为:![]() ,故D错误。答案选A。
,故D错误。答案选A。

【题目】闪锌矿(主要成分ZnS,含Cd、Fe、Cu等元素杂质)是冶炼锌单质的原料,有两种常见的冶炼方式:火法炼锌和湿法炼锌。两种方法均先将闪锌矿加热焙烧,得到以ZnO为主要成分的焙砂,再分别经过两条路线得到单质锌,同时得到副产品。
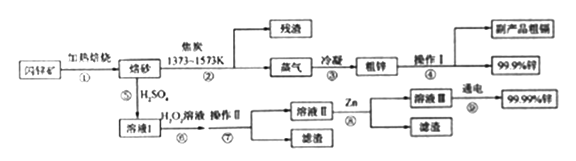
已知:
(I)相关金属单质的熔沸点
金属单质 | Zn | Fe | Cu | Cd |
熔点(K) | 693 | 1812 | 1356 | 594 |
沸点(K) | 1180 | 3023 | 2840 | 1040 |
(II)几种离子生成氢氧化物沉淀的pH
开始沉淀pH | 完全沉淀 pH | |
Fe3+ | l.l | 3.2 |
Zn2+ | 5.9 | 8.9 |
Cu2+ | 4.7 | 6.7 |
Cd2+ | 6.9 | 9.6 |
请回答下列问题:
(1)写出步骤①发生的主要反应的化学方程式___________________。
(2)步骤②若焦炭与ZnO(s)反应生成1mol CO时吸收akJ的热量,请写出该反应的热化学方程示________________。
(3)步骤④中操作I的分离方法为_______,得到副产品粗 镉需控制温度为_____左右。
(4)步骤⑦需调节溶液pH为_______,目的是__________。
(5)步骤⑨以Pt为阳极、Al为阴极进行电解的化学方程式为__________。
(6)分别取闪锌矿200kg,通过火法炼锌得到Zn的质量为65kg,通过湿法炼锌得到Zn的质量为78kg,闪锌矿中ZnS的质量分数约为________。
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得:
2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O +CO2↑。
I.制备碳酸亚铁:装置如图所示。
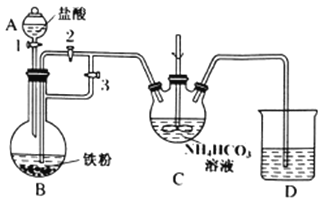
(1)C的名称是___________。
(2)清洗仪器,检查装置气密性,A中加入盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞______,打开活塞______;加入足量盐酸后,关闭活塞1,反应一段时间后,关闭活塞____,打开活塞_____。C中发生的反应的离子方程式为_______________。
Ⅱ.制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是______________。从所得溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发,________、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是_____________________。
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.760g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00mL,用0.1000mol/LCe(SO4)2标准溶液滴定至终点,记录数据如下表。
滴定次数 | 0.1000mol/LCe(SO4)2标准溶液体积/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁晶体的纯度为_________(以质量分数表示)。