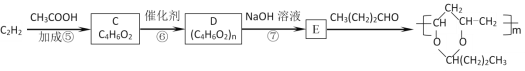题目内容
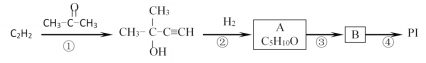
【题目】已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
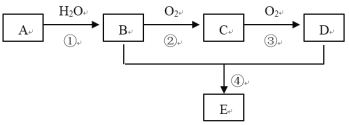
请回答下列问题:
(1)写出A的电子式 ___________。
(2)B、D分子中官能团的名称是 ___________。
(3)写出下列反应的化学方程式:
①________________;
②_________________;
④___________________,反应类型:_______。
(4)物质B可以被直接氧化为D,需要加入的试剂是___________。
【答案】![]() 羟基/羧基 CH2=CH2+H2O
羟基/羧基 CH2=CH2+H2O![]() CH3CH2OH 2CH3CH2OH+O2
CH3CH2OH 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3COOH+CH3CH2OH
2CH3CHO+2H2O CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 取代反应或酯化反应 酸性高锰酸钾溶液或酸性重铬酸钾溶液
CH3COOCH2CH3+H2O 取代反应或酯化反应 酸性高锰酸钾溶液或酸性重铬酸钾溶液
【解析】
A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,A和水发生加成反应生成B为CH3CH2OH,B被氧化生成C为CH3CHO,C被氧化生成D为CH3COOH,E是具有果香味的物质,且B和D发生酯化反应生成E,因此E为CH3COOCH2CH3。据此解答。
(1)乙烯分子中含有共价键,电子式为![]() ;
;
(2)乙醇分子中含有羟基,乙酸分子中羧基;
(3) 根据以上分析可知反应①是乙烯与水的加成反应,方程式为CH2=CH2+H2O![]() CH3CH2OH;反应②是乙醇的催化氧化,方程式为2CH3CH2OH+O2
CH3CH2OH;反应②是乙醇的催化氧化,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
反应④是酯化反应,方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,反应类型为取代反应或酯化反应;
CH3COOCH2CH3+H2O,反应类型为取代反应或酯化反应;
(4) 酸性高锰酸钾溶液或酸性重铬酸钾溶具有较强的氧化性,可以直接把乙醇氧化为乙酸。

练习册系列答案
相关题目