��Ŀ����
����Ŀ��һ���¶��£���2 L���ܱ������з������·�Ӧ��A(s)��2B(g)![]() 2C(g) ��H<0����Ӧ������B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����Ӧ��ƽ�����t1��t2��t3��t4ʱ�ֱ�ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2.�����й�˵����ȷ����
2C(g) ��H<0����Ӧ������B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����Ӧ��ƽ�����t1��t2��t3��t4ʱ�ֱ�ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2.�����й�˵����ȷ����

A. ��Ӧ��ʼ2 min�ڣ�v(B)��0.1 mol/(L��min)
B. t1ʱ�ı�����������������¶�
C. t3ʱ�ı�����������Ǽ�ѹ����ʱc(B)����
D. t4ʱ������ʹ���˴�������ʱc(B)����
���𰸡�D
��������A��ͨ��ͼ1��֪��v��B��= ="0.05" mol/��Lmin������A����
="0.05" mol/��Lmin������A����
B������ӦΪ���ȷ�Ӧ���������¶ȣ���Ӧ�����ƶ����������ʶ���С����������Ӧ�ٶȽ��͵ķ���С����B����
C����Ӧǰ����������ʵ������䣬����ѹǿ����������ƽ�ⲻ�ƶ������������С����ʱc��B�����C����
D��ʹ�ô������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����ʱc��B�����䣬��D��ȷ��

����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�����ȷ������ָ�����ϳɰ���ӦN2+3H2![]() 2NH3��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
2NH3��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�¶�/�� | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1�����ɱ������ݿ�֪�÷�ӦΪ______��Ӧ������������������������
�������ϣ�Ϊ������ƽ��ʱH2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______________������ĸ�������
a������ѹǿ b��ʹ�ú��ʵĴ���
c�������¶� d����ʱ����������е�NH3
��2��ԭ����H2��ͨ����ӦCH4��g��+H2O��g�� ![]() CO��g��+3H2��g����ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO��g��+3H2��g����ȡ����֪�÷�Ӧ�У�����ʼ������е�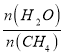 �㶨ʱ���¶ȡ�ѹǿ��ƽ��������CH4������Ӱ����ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ��������CH4������Ӱ����ͼ��ʾ��

��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ��p1________p2������>��������������<������
�ڸ÷�ӦΪ________��Ӧ��������������������������
��3��ԭ����H2����ͨ����ӦCO��g��+H2O��g�� ![]() CO2��g��+H2��g����ȡ��T ��ʱ�����ݻ��̶�Ϊ2 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO2��Ũ��Ϊ0.3 mol��L��1����ƽ��ʱCO��ת����Ϊ________
CO2��g��+H2��g����ȡ��T ��ʱ�����ݻ��̶�Ϊ2 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO2��Ũ��Ϊ0.3 mol��L��1����ƽ��ʱCO��ת����Ϊ________